
【题目】宏观和微观相联系是化学独特的思维方式。
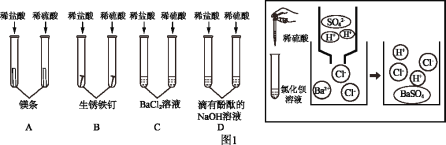
(1)物质性质反映其组成和结构。从宏观进入微观,探索物质变化规律。
①不同酸具有相似的化学性质,但性质也存在差异。图1中不能体现酸的通性的是_____(填字母序号,下同);写出B中稀盐酸与铁锈反应的化学方程式_____;C中稀盐酸不能与氯化钡溶液反应,而稀硫酸则能与之反应生成白色沉淀,据图从微粒的角度分析写出该反应的实质是_____。
②一杯水中氢元素与氧元素的质量比和1个水分子中氢原子与氧原子的质量比_____(填“相等”或“不相等”)。
(2)物质组成和结构决定其性质。从微观进入宏观,探索物质变化规律。
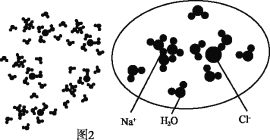
①图2圆圈中表示这杯氯化钠溶液的构成,则该氯化钠溶液中溶质和溶剂的质量比是_____。
②通过分析组成和结构,可以预测物质的某些性质。根据图3硫酸氢钠溶液的微观图示,分析推测NaHSO4的性质,其中合理的是_____。
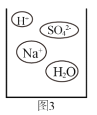
A 其水溶液能使紫色石蕊试液变红
B 其水溶液能与金属锌反应生成氢气
C 其水溶液能与硝酸钡溶液反应生成硫酸钡沉淀
D 其水溶液能与金属镁发生置换反应,得到金属钠
【答案】C Fe2O3+6HCl=2FeCl3+3H2O 溶液中的Ba2+和SO42-反应生成BaSO4沉淀 相等 13:40 ABC
【解析】
(1)①酸的通性是溶液中H+体现的,C中参与反应的是SO42-,所以没有体现酸的通性。硫酸和BaCl2溶液反应的微观本质从图中可以看出是溶液中的Ba2+和SO42-反应生成BaSO4沉淀。B中稀盐酸与铁锈反应生成氯化铁和水,其化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O;C中稀盐酸不能与氯化钡溶液反应,而稀硫酸则能与之反应生成白色沉淀,根据图从微粒的角度可知,其反应的实质是:溶液中的Ba2+和SO42-发生复分解反应生成BaSO4沉淀和HCl;故填:C;Fe2O3+6HCl=2FeCl3+3H2O;溶液中的Ba2+和SO42-反应生成BaSO4沉淀
②一杯水中由水组成,氢元素与氧元素的质量比为2:16和1个水分子中氢原子与氧原子的质量比为2:16;故填:相等
(2)①从图中可以看出,每个Na+和Cl-周围共有10个水分子,所以溶液中溶质和溶剂的质量比是58.5:(18×10)=13:40;故填:13:40
②NaHSO4溶液中含有Na+、H+、SO42-三种离子,因此NaHSO4溶液的性质由三种离子来体现,A、B选项是H+的性质,C选项是SO42-的性质;Mg不能置换出Na,说法错误。故填:ABC


科目:初中化学 来源: 题型:
【题目】将160g氧化铁粉末放于硬质玻璃管进行实验室模拟炼铁实验。测得管内剩余固体质量、参与反应的CO质量随温度变化的曲线如图所示,请计算:
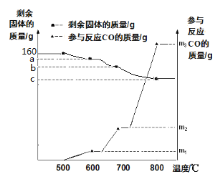
[资料]氧化铁被高温还原是逐步失去氧元素的,其过程为:
![]()
则下列说法正确的是:
A. 当固体质量为a时,参加反应的CO的质量为m3
B. 实验结束后,可用磁铁和稀盐酸检验c处的产物
C. a-b=16
D. m1:m2:m3为1:3:9
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某食用纯碱中含有少量的氯化钠,为测定该纯碱中碳酸钠(Na2CO3)的含量,现取该纯碱样品12.5 g,加入150.0 g稀盐酸溶液恰好完全反应,测得反应后溶液总质量变成158.1 g。请计算:
(1)反应中产生CO2的质量为_________ 克。
(2)纯碱样品中Na2CO3的质量分数___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图的有关信息,下列说法正确的是

A. 镁离子(Mg2+)的核内有12个质子B. 镁离子与氯离子的电子层数相同
C. 氯原子的核电荷数为35.45D. X=8时,该微粒带一个单位正电荷
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是

A. 参加反应的甲和乙质量比为 12:19
B. 丙可能是该反应的催化剂
C. x 的值是 7
D. 丁可能是化合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知2CO2+2Na2O2=2Na2CO3+O2,在密闭容器中,将17.6gCO2与少量Na2O2固体充分 反应后,气体变为12g。下列说法正确的是
A. 12g气体全部是O2
B. 12g气体通过足量NaOH溶液后,气体减少8.8g
C. 反应后的固体是混合物
D. 生成Na2CO3的质量为26.5g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素周期表将已知元素科学有序地排列起来,便于我们研究它们的性质和用途。下表表示元素 周期表的一部分,请回答下列问题。

(1)元素在周期表中的分布是有规律的,表中①②③所代表的三种元素中,属于非金属的是 。
(2)表中氮元素的化合价有多种,请写出化合价为十1价的氮的氧化物 (用化学式表示)
(3)随着新元素的不断发现,元素周期表还将逐渐完善。最近,科学家用大量高速钙原子轰击锫原子,形成了117号元素的原子,该元素原子核中一定含有117个 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】草酸是一种酸,草酸晶体(H2C2O42H2O)易溶于水,熔点较低,加热会熔化、气化和分解。草酸(H2C2O4)与氢氧化钙的反应:H2C2O4+Ca(OH)2=CaC2O4↓(白色)+2H2O。
(分析讨论)
实验室可用加热草酸晶体分解的方法获得CO
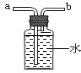
(1)先加热草酸晶体生成CO、CO2和H2O,其化学方程式是_____;
(2)最后用如图装置收集CO,气体应从_____端进入(选填“a”或“b”)。
(实验反思)
(3)甲认为如图中试管口应略向下倾斜,老师、同学讨论后一致认为装置是正确的,理由是_____。

(4)实验中观察到澄清石灰水变浑浊,乙认为一定是由草酸晶体受热分解产生的CO2所导致,丙认为乙的结论不严密,理由是_____。
(生活链接)菠菜营养丰富,但菠菜豆腐同食,易得结石(主要成分草酸钙晶体),小组同学对草酸钙晶体的性质及组成产生了兴趣。
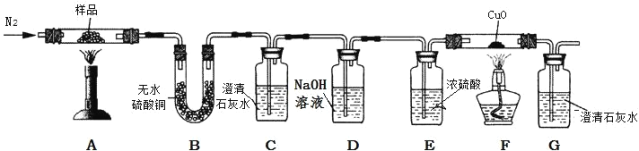
(性质探究)按下图装置将草酸钙晶体(CaC2O4·xH2O)样品高温加热,使其完全分解并检验产生的气体。
(问题讨论)
(5)B中观察到_____现象,说明反应生成了水;
(6)C、G中澄清石灰水均变浑浊,说明反应还生成_____和_____气体。
(7)有同学认为上述结论不严谨,并不能得出有一氧化碳生成的结论。请说明理由_____。
(组成确定)
(8)利用热分析仪对草酸钙晶体(CaC2O4·xH2O)进行热分解,获得相关数据,绘制成固体质量—分解温度的关系如图。

①温度为200℃左右时,晶体全部失去结晶水,晶体中结晶水的质量为_____g。
②计算CaC2O4·xH2O中的x(CaC2O4的相对分子质量:128),x=_____。
③800℃以上时,经检验残留固体为氧化物,图中m的值是_____。
④写出固体质量由12.8g变为10.0g时的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018年5月13日,我国首艘国产航母开始海试,标志着我国在航海及军事领域取得重大突破。
(1)建造航母的特种钢中含有金属钛,构成金属钛的粒子是_____(填“原子”、“分子”或“离子”),工业制钛有一种反应为:TiF4+2X=4HF+2SO3+TiO2,X的化学式为_____。
(2)特种钢是铁的一种合金,工业上可用赤铁矿和一氧化碳来炼铁,化学方程式为_____。
(3)航母外壳用涂料覆盖可以有效防止钢铁的锈蚀,原因是_____:除了防止金属的锈蚀以外,请再写一条保护金属资源的有效方法或途径_____。
(4)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验方案,其中能达到目的是_____
A FeSO4溶液、Zn、Cu
B ZnSO4溶液、稀盐酸、Fe、Cu
C ZnSO4溶液、FeSO4溶液、Cu
D ZnCl2溶液、CuCl2溶液、Fe
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com