
| A. | >7 | B. | <7 | C. | =7 | D. | 无法确定 |
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 16% | B. | 22% | C. | 32% | D. | 46% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
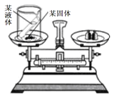 某科学兴趣小组的同学利用如图所示实验装置验证质量守恒定律. 则小试管中的液体和烧杯中的固体应分别选用( )
某科学兴趣小组的同学利用如图所示实验装置验证质量守恒定律. 则小试管中的液体和烧杯中的固体应分别选用( )| A. | 水和氯化钠固体 | B. | 氢氧化钙溶液和碳酸钠粉末 | ||
| C. | 稀盐酸和铁粉 | D. | 5%双氧水和二氧化锰粉末 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 所含杂质 | 除杂质的方法 |
| A | 二氧化锰 | 氯化钠 | 加水溶解,过滤,蒸发结晶 |
| B | 氯化钠溶液 | 碳酸钠 | 加入过量稀盐酸,加热蒸发 |
| C | 氯化钙溶液 | 稀盐酸 | 加入过量氢氧化钙,过滤 |
| D | 氢氧化钠溶液 | 碳酸钠 | 加入适量的石灰水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 实验序号 | 1 | 2 | 3 | 4 | 5 |
| 加入稀盐酸的质量/克 | 9.8 | 9.9 | 10.0 | 10.1 | 10.2 |
| 溶液的pH | 12.1 | 11.8 | 7.0 | 2.2 | 1.9 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 今年6月8日至14日是全国节能宣传周,活动主题是“携手节能低碳,共建碧水蓝天”.根据如图碳循环的部分过程进行的有关分析中,错误的是( )
今年6月8日至14日是全国节能宣传周,活动主题是“携手节能低碳,共建碧水蓝天”.根据如图碳循环的部分过程进行的有关分析中,错误的是( )| A. | ②是指生产者、消费者和分解者的呼吸作用 | |
| B. | 在生物群落的食物链中,碳是以二氧化碳的形式进行传递的 | |
| C. | 在城市交通中少开汽车多骑自行车能减少①过程的发生 | |
| D. | 绿化环境、爱护草木有利于③过程的进行 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com