
| A. | Zn | B. | Mg | C. | Al | D. | 以上答案都不对 |
分析 采用极值法先计算纯铁5.6g能生成氢气的质量,然后再确定杂质的类别.假设样品中全部是铁,计算一下5.6g铁能产生多少氢气,再与0.195g作比较,若计算值比0.195g大,说明混有的金属产生氢气的能力不如铁,或者说根本就不会产生氢气;若计算值比0.195g小,说明混有的金属产生氢气的能力比铁强.
解答 解:设纯铁5.6g能生成氢气的质量为x,则有
Fe+H2SO4=FeSO4+H2↑
56 2
5.6g x
$\frac{56}{2}$=$\frac{5.6g}{x}$,x=0.2g
设纯锌5.6g能生成氢气的质量为b,则有
Zn+H2SO4=ZnSO4+H2↑,
65 2
5.6g b
$\frac{65}{2}$=$\frac{5.6g}{b}$,b≈0.17g
设纯镁5.6g能生成氢气的质量为z,则有
Mg+H2SO4=MgSO4+H2↑
24 2
5.6g z
$\frac{24}{2}$=$\frac{5.6g}{z}$,z≈0.47g
设纯铝5.6g能生成氢气的质量为a,则有
2Al+3H2SO4=Al2(SO4)3+3H2↑
54 6
5.6g a
$\frac{54}{6}$=$\frac{5.6g}{a}$,a≈0.62g
根据平均值法,若是铁与镁或铝的混合物,则生成的氢气质量应该大于0.2g,不可能为0.195g,故混有的杂质是锌.
故选A.
点评 本题考查了混合金属与酸反应生成氢气的质量关系,完成此类题目,可以首先采用极值法,然后采用平均值法进行.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 漏斗,玻璃棒 | B. | 大试管,集气瓶 | ||
| C. | 酒精灯,铁架台 | D. | 导气管,单孔橡胶塞 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 金属材料 | B. | 复合材料 | C. | 有机高分子材料 | D. | 无机非金属材料 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水能灭火,所以电器着火应立即用水浇灭 | |
| B. | 镁条在空气中燃烧后的固体质量大于镁条的质量,所以该反应不符合质量守恒定律 | |
| C. | 酸和碱能发生中和反应,故硝酸与氢氧化钠也能发生中和反应 | |
| D. | 碳酸盐能与稀盐酸反应放出气体,故能与稀盐酸反应放出气体的物质一定是碳酸盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
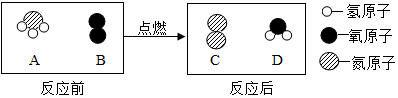
| A. | A中各元素的质量比为14:1 | B. | A中氮元素的化合价为+3 | ||
| C. | 该反应中B和C的质量比为12:7 | D. | 该反应中A和D 的分子个数比为1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 解释与结论 |
| 取澄清溶液A逐滴滴入一定量氢氧化钠溶液 | 开始无明显现象,后产生白色沉淀 | 原因是HCl+NaOH=NaCl+H2O, AlCl3+3NaOH=Al(OH)3↓+3NaCl. (用化学方程式表示) |
| 继续滴入氢氧化钠溶液直至过量 | 沉淀溶解 | 摩擦剂中还含有Al(OH)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com