
| A. | 氢氧化钠 | B. | 碳酸钾 | C. | 氯化钠 | D. | 硝酸银 |
分析 根据复分解反应发生的条件可知,若物质之间相互交换成分不能生成水、气体、沉淀,则能够在溶液中大量共存;某溶液中含有盐酸,则能存在于该溶液中的物质不能与盐酸发生化学反应,据此进行分析判断即可.
解答 解:A、稀盐酸和氢氧化钠在溶液中能相互交换成分生成氯化钠和水,不能存在于该溶液中,故选项错误.
B、碳酸钾和盐酸反应生成氯化钠、水和二氧化碳,不能存在于该溶液中,故选项错误.
C、氯化钠与稀盐酸不反应,可以大量存在于该溶液中,故选项正确.
D、HCl和AgNO3在溶液中能相互交换成分生成氯化银沉淀和硝酸,不能存在于该溶液中,故选项错误.
故选:C.
点评 本题考查物质的共存问题,判断物质在溶液中能否共存,主要看溶液中的各物质之间能否发生反应生成沉淀、气体、水.


科目:初中化学 来源: 题型:解答题
| 项目 | 标准 |
| 感官指标 | 无异味、异臭等 |
| 化学指标 | pH6.58.5,铜<1.0mg•L 1,铁<0.3mg•L-1,氟化物<1.0mg•L-1游离氯≥0.3mg•L-1等 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 野炊过程实际上是运用科学知识分析、解决问题的过程,该项活动过程中涉及许多科学知识的运用.某次野炊活动中,同学们携带了铁锅、豆腐、牛肉、面条、西红柿、食用油、食盐、味精、食醋、洗涤用碱(有效成份为碳酸钠)等物品.
野炊过程实际上是运用科学知识分析、解决问题的过程,该项活动过程中涉及许多科学知识的运用.某次野炊活动中,同学们携带了铁锅、豆腐、牛肉、面条、西红柿、食用油、食盐、味精、食醋、洗涤用碱(有效成份为碳酸钠)等物品.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
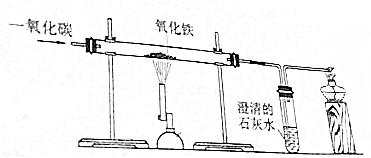
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
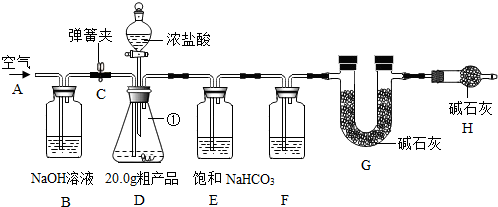
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com