
 2012年1月15日,广西龙江河发生镉污染事件,如图是镉元素在元素周期表中的信息,从该图获取的信息中,正确的是( )
2012年1月15日,广西龙江河发生镉污染事件,如图是镉元素在元素周期表中的信息,从该图获取的信息中,正确的是( )| A. | 镉原子的核外有48个电子 | B. | 镉元素的原子序数为112 | ||
| C. | 镉元素属于非金属元素 | D. | 镉元素相对原子质量为112.4g |
分析 根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可.
解答 解:A、根据元素周期表中的一格可知,左上角的数字为48,表示原子序数为48;根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为48,故选项说法正确.
B、根据元素周期表中的一格可知,左上角的数字为48,该元素的原子序数为48,故选项说法错误.
C、根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是镉,属于金属元素,故选项说法错误.
D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为112.4,相对原子质量单位是“1”,不是“克”,故选项说法错误.
故选:A.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)进行分析解题的能力.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 区分热固性塑料和热塑性塑料--加热,观察外形变化 | |
| B. | 区别硝酸钾和硝酸铵--用熟石灰 | |
| C. | 鉴别NaOH、K2CO3、BaCl2三种白色固体--用稀H2SO4 | |
| D. | 检验CaO中是否含有Ca(OH)2--加水后滴加酚酞溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
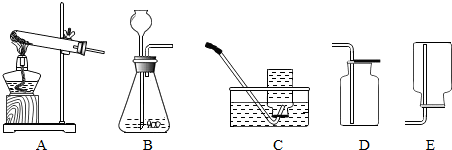
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作和步骤 | 实验现象与结论 |
| (1)用4支试管,各取少量四种溶液,分别滴加紫色石蕊试剂; | 一支试管中溶液变为红色,则原溶液是稀盐酸. |
| (2)另用3支试管,各取少量未确定的三种溶液,分别滴加步骤(1)检验出的溶液. | 一支试管中溶液有气泡放出,则原溶液是Na2CO3溶液 |
| (3)另用2支试管,各取少量未确定的二种溶液,分别滴加步骤(2)检验出的溶液 | 一支试管溶液中有白色沉淀析出,则原溶液是Ca(OH)2溶液,其反应的化学方程式 为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;剩下的就是最后一种溶液. |
| 同学 | 实验操作 | 实现现象 | 结论 |
| 小红 | 用3支试管,各取少量三种溶液,分别滴加另一种溶液. | 一支试管溶液中有气泡放出,其余两支试管溶液中无现象. | 所滴加的溶液是稀盐酸. |
| 小勇 | 一支试管溶液中有白色沉淀析出,其余两支试管溶液中无现象. | 所滴加的溶液是Na2CO3溶液. | |
| 小新 | 三支试管溶液中都无现象. | 所滴加的溶液是NaOH溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
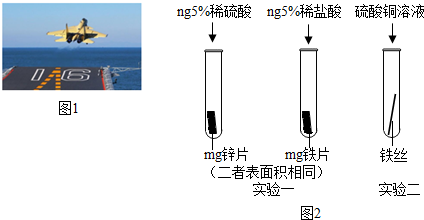
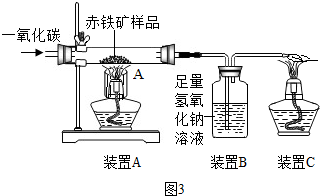
| 实验步骤 | 实验现象 | 实验结论 |
| 分别取少量硫酸铜溶液、硫酸锌溶液于两支试管中,将铁丝分别浸入两溶液中,观察现象 | 浸入硫酸铜溶液中的铁丝表面出现红色固体,溶液由蓝色逐渐变为浅绿色;浸入硫酸锌溶液的铁丝无明显变化 | 金属活动性顺序: Zn>Fe>Cu |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com