
分析 (1)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写;根据生铁和钢都是铁的合金,根据它们的组成进行分析解答即可.
(2)铝易与空气中的氧气反应生成氧化铝,氧化铝具有致密结实的结构,氧化铝和铝均能与稀硫酸发生反应.
解答 解:(1)高温条件下一氧化碳能把铁从磁铁矿石(主要成分为Fe304)中还原出来,生成铁和二氧化碳,反应的化学方程式为:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.生铁是含碳量为2%~4.3%的铁合金,钢是含碳量为0.03%~2%的铁合金,其中含碳量较高的是生铁.故填:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;生铁;
(2)铝的活动性较强,易与空气中的氧气反应生成致密结实的氧化铝薄膜,当将一块未经打磨的铝片放入足量的稀硫酸中,表面的氧化铝先与稀硫酸反应生成硫酸铝和水,然后铝与稀硫酸反应生成硫酸铝和氢气.故填:Al2O3;Al2O3+3H2SO4=Al2(SO4)3+3H2O,2Al+3H2SO4=Al2(SO4)3+3H2↑.
点评 本题考查了炼铁的原理、铁合金的碳含量、金属铝的氧化以及化学方程式的书写,属于基本知识的考查.


科目:初中化学 来源: 题型:填空题
 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点. 据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点. 据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 测定四种气体的密度 | B. | 用燃着的木条检验 | ||
| C. | 向瓶中倒入石灰水 | D. | 试验四种气体的溶解度 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
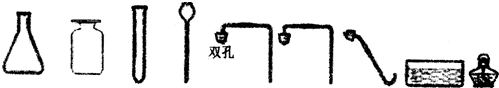
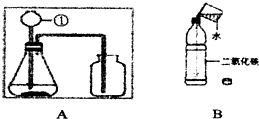

查看答案和解析>>
科目:初中化学 来源: 题型:多选题
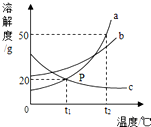
| A. | t2℃时a、b两种物质饱和溶液降温到t1℃时,析出晶体质量a>b | |
| B. | t2℃时,将50g a物质放入50g水中充分溶解得到100g a的饱和溶液 | |
| C. | 将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数关系是b>a>c | |
| D. | 将c的饱和溶液变为不饱和溶液,可采用降温的方法 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
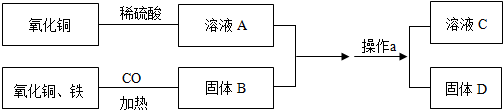
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 实验时,用剩的药品要放回到原试剂瓶中,以免浪费 | |
| B. | 实验时,如果没有说明液体药品的用量时,应取1~2 mL | |
| C. | 给试管里的液体加热时,试管要与桌面成45度角 | |
| D. | 取用粉末状固体药品时可用药匙 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
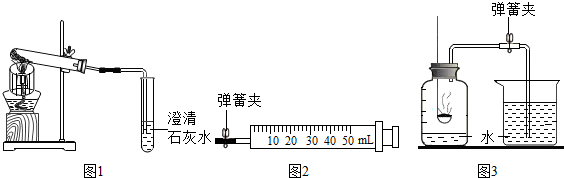
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO2气体用NaOH溶液来吸收中 | B. | 稀盐酸滴入氯化钠溶液中 | ||
| C. | 氢氧化钠溶液滴入硫酸铜溶液中 | D. | 硫酸钠溶液滴入氯化铜溶液中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com