
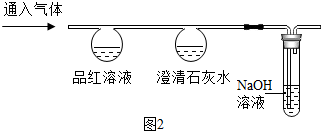
| ʵ��� | ʵ��� | |
| ͨ��CO2 | ͨ��SO2 | |
| Ʒ����Һ | �����Ա仯 | ��ɫ��Ϊ��ɫ |
| ����ʯ��ˮ | ��ɫ���� | ��ɫ���� |
| SO2���Ũ����ֵ����λmg/m3�� | ||
| һ���� | ������ | ������ |
| 0.15 | 0.50 | 0.70 |
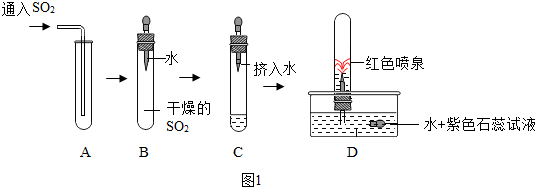
���� ���ݷ���װ�õ�ѡ�����ݽ�𣻸���ʵ������ȷ������������������ʣ��������������������Ʒ�Ӧ����������ƺ�ˮ���������ʵ����ʽ��ʵ��������з�����ɣ�
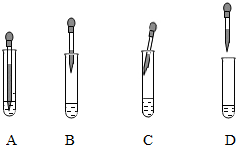
��� �⣺��1��ѡ����װ����ҪӦ�ÿ��ǵ������Ƿ�Ӧ���״̬����Ӧ���������AB��
��2������ʵ�������Ʋ�SO2�����ܶȱȿ�����������ˮ��������������ܶȱȿ�����������������ˮ��
��3���ٶ��������������ʯ��ˮ��Ӧ������������ƣ�CaSO3����ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ��Ca��OH��2+SO2�TCaSO3��+H2O�����Ca��OH��2+SO2�TCaSO3��+H2O��
��ʵ�����NaOH��Һ������β������ֳ����������Ⱦ�������������β������ֹ����Ⱦ������
���������ϡ��ڶ����������ˮ��Ӧ�Ļ�ѧ����ʽΪ��SO2+I2+2H2O=H2SO4+2HI��
��4���ٵ�������������ʵ���Һ����ɫ�����ɫʱ��Ӧǡ����ȫ���������
��1g������������Ϊ0.0127%�ĵ�ˮ�к��е������Ϊ��1000mg��0.0127%=0.127mg����ָ���ص���ע������ȡ����140��ע�������Թ��У�����ÿ�γ���500mL������������Ϊ��140��5��10-4=0.07��m3��
��������������Ϊx
SO2 +I2 +2H2O�TH2SO4+2HI
64 254
x 0.127mg
$\frac{64}{254}=\frac{x}{0.127mg}$
x=0.032mg
�ɴ˿ɼ��������SO2�ĺ���Ϊ��$\frac{0.032mg}{0.07{m}^{3}}$=0.46mg/m3������ص�Ŀ�����SO2�ĺ������ڶ����������0.46��������
���� ���⿼����dz�����������ʵ�ʵ��̽���Լ����ݻ�ѧ����ʽ�ļ����֪ʶ����ɴ��⣬�����������е�֪ʶ���У�


 ������������ϵ�д�
������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ˮ�õ�H2��O2����֪ˮ������ԭ�Ӻ���ԭ����ɵ� | |
| B�� | �������ù��˵ķ������Խ���ˮ��Ӳ�� | |
| C�� | ��ˮ�ķ����г��������ˡ����������� | |
| D�� | ��������ˮ��������ˮ�Ǵ�ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
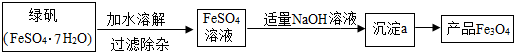
 A��F��Ϊ���л�ѧ���������ʣ���֪��A��C�����Ԫ����ȫ��ͬ�Ļ����Cͨ��ΪҺ�壬DΪ��ɫ���壬F�ǰ�ɫ���ܹ��壬���н���Ԫ�ص���������Ϊ40%������֮������ͼ��ʾ��ת����ϵ���������ʺͷ�Ӧ��������ȥ����
A��F��Ϊ���л�ѧ���������ʣ���֪��A��C�����Ԫ����ȫ��ͬ�Ļ����Cͨ��ΪҺ�壬DΪ��ɫ���壬F�ǰ�ɫ���ܹ��壬���н���Ԫ�ص���������Ϊ40%������֮������ͼ��ʾ��ת����ϵ���������ʺͷ�Ӧ��������ȥ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʳ������״�����ζ�� | |
| B�� | �ž��Ժ��л�ѧ���ʵ�ʳƷ | |
| C�� | �����������Ŀ������� | |
| D�� | �ڲ�ͨ�����������ȼ����ˮ��ϴ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Զ��ױ������л��߷��ӻ����� | |
| B�� | �Զ��ױ���̼Ԫ�ص������������ڼ�����̼Ԫ�ص��������� | |
| C�� | �Զ��ױ�����8��̼ԭ�Ӻ�10����ԭ�ӹ��� | |
| D�� | �Զ��ױ���̼Ԫ�ء���Ԫ�ص�������Ϊ4��5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
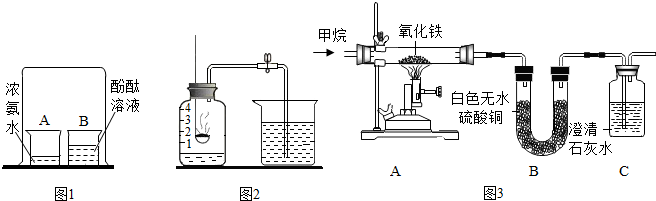
| ʵ �� �� �� | ʵ �� �� �� |
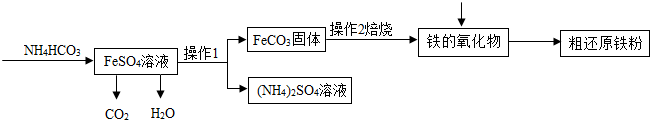
| A�к�ɫ��ĩ��Ϊ��ɫ�� B�а�ɫ��ˮ����ͭ����ɫ�� C�г���ʯ��ˮ����ǣ� | ��Ӧ�IJ���Ϊ������̼��ˮ�� ������л�ԭ�ԣ�A�з�Ӧ�Ļ�ѧ����ʽΪ 3CH4+4Fe2O3$\frac{\underline{\;����\;}}{\;}$8Fe+6H2O+3CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
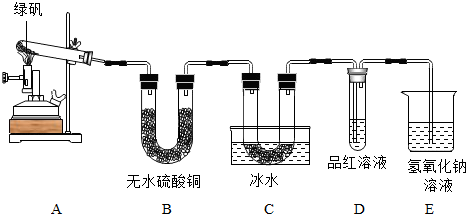
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com