
| 结果编号 | ① | ② |
| 计算结果 | 14.2% | 7.1% |
分析 根据氢氧化钠与稀硫酸的质量比分析反应的情况,根据方程式求出生成的硫酸钠,再求出所得溶液中硫酸钠的质量分数.
解答 解:由2NaOH+H2SO4═Na2SO4 +2H2O可知,氢氧化钠与硫酸的反应的质量为80:98,当100g溶质质量分数为8%的氢氧化钠溶液于烧杯中,向其中加入100g19.6%的稀硫酸,氢氧化钠与硫酸的质量为:(100g×8%):(100g×19.6%)=80:196,所以,硫酸有剩余,应根据氢氧化钠的质量计算.
设生成生的硫酸钠的质量为x
2NaOH+H2SO4═Na2SO4 +2H2O
80 142
100g×8% x
$\frac{80}{142}=\frac{100g×8%}{x}$ 解得:x=14.2g,
所得溶液中硫酸钠的质量分数:$\frac{14.2g}{100g+100g}×100%$=7.1%
由以上计算可知,赞同的计算结果是②.
故答为:(1)②;(2)见上边计算.
点评 本题属于根基方程式的计算,解题的关键是正确地判断完全反应的量,应根据次量进行计算.


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:初中化学 来源: 题型:选择题
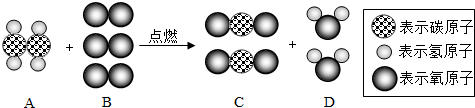
| A. | 该反应属于置换反应 | |
| B. | 参加反应的A、B两物质的分子个数比为1:3 | |
| C. | 生成物中C物质与D物质的质量比为11:9 | |
| D. | 反应前后氧元素的化合价没有改变 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
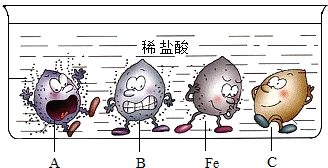
| A. | C可能是铜 | |
| B. | 将Fe放在B的盐溶液中可以置换出B | |
| C. | 四种金属的活动性顺序是:A>B>Fe>C | |
| D. | 钢和生铁都是铁合金 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 均一稳定的液体一定是溶液 | |
| B. | 检测酒驾的重铬酸钾(K2Cr2O7)中铬元素的化合价为+7价 | |
| C. | 硫在氧气中燃烧产生明亮的蓝紫色火焰 | |
| D. | 厨房发生燃气泄漏应马上开灯检查 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com