
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案科目:初中化学 来源: 题型:推断题
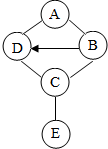 如图中A、B、C、D、E是初中化学常见的五种不同类别的物质,E是导致温室效应的一种气体,图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略)
如图中A、B、C、D、E是初中化学常见的五种不同类别的物质,E是导致温室效应的一种气体,图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略)查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 溶剂 | 水 | 酒精 |
| 溶解度 | 1.0 | 0.5 |
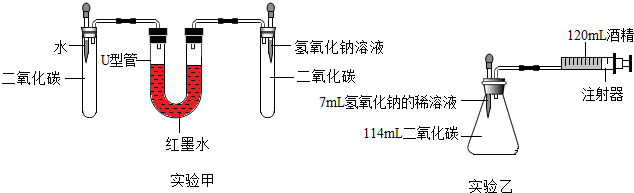
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
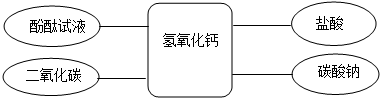 归纳总结是学习化学的重要方法,某化学兴趣小组学习碱的性质后,通过实验对氢氧化钙的化学性质进行了验证和总结,如图所示“--”表示物质两两之间能发生化学反应.请根据如图,回答问题.(已知:CaCl2溶液呈中性,CaCl2+Na2CO3═CaCO3↓+2NaCl)
归纳总结是学习化学的重要方法,某化学兴趣小组学习碱的性质后,通过实验对氢氧化钙的化学性质进行了验证和总结,如图所示“--”表示物质两两之间能发生化学反应.请根据如图,回答问题.(已知:CaCl2溶液呈中性,CaCl2+Na2CO3═CaCO3↓+2NaCl)查看答案和解析>>
科目:初中化学 来源: 题型:选择题
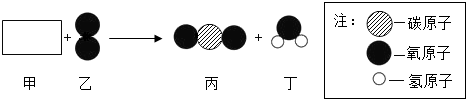
| A. | 甲物质的化学式为CH2O | |
| B. | 除甲以外其他物质都是氧化物 | |
| C. | 生成的丙、丁两物质的质量比是22:9 | |
| D. | 反应前后分子个数不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
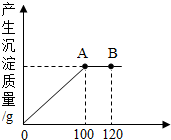 管理员在学校实验室发现了一瓶敞口放置的氢氧化钠溶液,同学小晴认为该溶液已部分变质成Na2CO3,为探究溶液中溶质的成分,请回答下列问题.
管理员在学校实验室发现了一瓶敞口放置的氢氧化钠溶液,同学小晴认为该溶液已部分变质成Na2CO3,为探究溶液中溶质的成分,请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验 | 现象 | 解释或结论 | |
| 实验一 | 将适量的水垢和水装入试管中,充分振荡后静置,用滴管取上层清液于小试管中,然后再向小试管中滴入紫色石蕊溶液 | 紫色石蕊溶液不变色 | Ca(OH)2微溶于水,其水溶液显碱性,能使紫色石蕊溶液变蓝色,不变色说明水垢中一定没有Ca(OH)2 |
| 实验二 | 按如图所示方案进行实验 | 反应一段时间后水垢消失,溶液澄清;玻璃片上澄清石灰水变浑浊 | 石灰水变浑浊,说明有CO2生成,则水垢中一定含有CaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
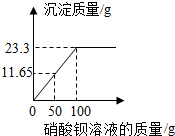 某学校兴趣小组在参与“五水共治”行动中,考察了某工厂的废水处理工程,并取该厂未经处理的废水样品进行测定分析:
某学校兴趣小组在参与“五水共治”行动中,考察了某工厂的废水处理工程,并取该厂未经处理的废水样品进行测定分析:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 煅烧越充分则消耗盐酸越少 | |
| B. | 整个反应过程中产生的二氧化碳总质量22克 | |
| C. | 煅烧后固体中氧元素质量分数减小 | |
| D. | 反应结束后共生成55.5克氯化钙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com