
【题目】某同学为了测定生铁样品中铁的质量分数,将60g稀盐酸分3次加入到盛有4g该样品的烧杯中(样品中只有铁已稀盐酸反应),所得数据如下表,则下列说法中正确的是
A. 第1次和第2次产生的氢气质量不相等 B. 第2次和第3次剩余固体中均有铁
C. 第3次反应后溶液中的溶质是FeCl3 D. 生铁样品中铁的质量分数是97.5%
 互动英语系列答案
互动英语系列答案科目:初中化学 来源: 题型:
【题目】(1)用适当的数字和化学符号填空:
①2个氢原子_________; ②氯化钠中的阴离子________;③保持水化学性质的最小微粒__________; ④氧化镁中镁元素的化合价_________;⑤地壳中最多的金属元素与非金属元素形成的化合物_________;⑥实验室检验二氧化碳气体____________。
(2)根据右图回答下列问题:
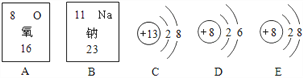
①钠元素与氧元素的本质区别是___________;
②A、B 两种元素组成的化合物的化学式为____________
③C、D、E中属于离子的是___________
(3)用“>”或“=”或“<”或“≥”或“≤”填空:
① a mL酒精中加入b mL水,混合后的体积为c mL,则a+b________c。
② a克铁与b克氧气充分反应,得到c克四氧化三铁,则a+b_________c。
(4)小明用蜡烛进行了下列探究活动。
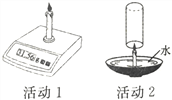
活动1:点燃蜡烛后,电子称示数逐渐减小,蜡烛减小的质量_________(填“大于”“等于”或“小于”)燃烧后生成物的总质量.
活动2:用玻璃杯迅速扣住燃烧的蜡烛,并使杯口始终浸没在水中,下列说法正确的是_____(填序号)
A.可观察到蜡烛熄灭
B.最终杯中液面高于碗中液面
C.该方法能准确测定空气中氧气的含量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学方程式符合题意且书写正确的是( )
A. 铝丝浸入硫酸铜溶液中:2Al+3CuSO4===3Cu+Al2(SO4)3
B. 生活中用天然气作燃料:C2H5OH + 3O2![]() 2CO2 + 3H2O
2CO2 + 3H2O
C. 铁与稀硫酸反应:2Fe+3H2SO4==3H2↑+Fe2(SO4)3
D. 用大理石和盐酸制取二氧化碳:CaCO3 + 2HCl = CaCl2 + H2O + CO2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钠是一种活泼金属,常温下能与氧气、水等物质发生反应。钠与水反应的化学方程式为:2Na+2H2O===2NaOH+H2↑。在实验室,某同学先取50 mL一定质量分数的硫酸铜溶液于烧杯中,再取绿豆大小的钠投入硫酸铜溶液中,充分反应后过滤,得到滤液和蓝色滤渣,并对滤液的成分进行探究。
(提出问题)滤液中溶质的成分是什么?
(查阅资料)Na2SO4溶液呈中性。
(猜想与假设)
猜想一:Na2SO4
猜想二:Na2SO4和NaOH
猜想三:Na2SO4和CuSO4
猜想四:Na2SO4、CuSO4和NaOH
其中猜想不合理的是________,理由是________(用化学方程式表示)。
(实验方案与验证)
实验 | 实验操作 | 实验现象 | 实验结论 |
实验一 | 取少量滤液于试管中,观察现象 | 溶液为无色 | 猜想___不成立 |
实验二 | 另取少量滤液于试管中,向其中 加入__________ | 无明显现象 | 猜想二不成立 |
实验三 | 常温下,再取少量滤液,测溶液 酸碱度 | pH=7 | 猜想____成立 |
(拓展延伸)
(1)将2.3g金属钠与足量水反应,可得到氢氧化钠______g。
(2)金属钠在保存中应注意的是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组为了测定黄铜(铜、锌合金)的组成。在化学老师的帮助下,选用98%的浓硫酸、黄铜样品进行下列实验并计算。

实验Ⅰ:配制150g 9.8%的稀硫酸。
(1)计算:需要浓硫酸约8.2mL;需要水的体积为_________mL(取整数值)
(2)量取浓硫酸和水:用量筒量取8.2 mL浓硫酸和一定体积的水。如果量取98%的浓硫酸时俯视读数,会导致所配溶液溶质质量分数_________9.8%(填“大于”、“小于”或“等于”)。
(3)_________ 。(4)装瓶贴标签。
实验Ⅱ:用下图1所示装置测定锌铜合金中锌、铜的质量分数。
(1)实验前,先将锌铜合金用砂纸打磨,其目的是:_________;
(2)实验操作步骤有:①记录量气管D的液面位置;②检查气密性,将药品和水装入各仪器中,连接好装置。③待B中不再有气体产生并恢复至室温后,记录量气管D的液面位置;④由A向B滴加足量试剂;⑤将B中剩余固体过滤,洗涤,干燥,称重;上述进行的操作的顺序是_________(填序号);记录量气管D的液面位置时,除视线平视外,还应_________;
(3)B中发生反应的化学方程式为_________;
(4)若实验中,锌铜合金与稀硫酸充分反应后,测得产生的气体体积为V L,为求出合金中锌、铜的质量分数,还要用到下列数据中的_________;
A.加入的稀硫酸的质量分数 B.反应后B中剩余固体的质量
C.实验前反应装置中空气的体积 D.实验条件下氢气的密度
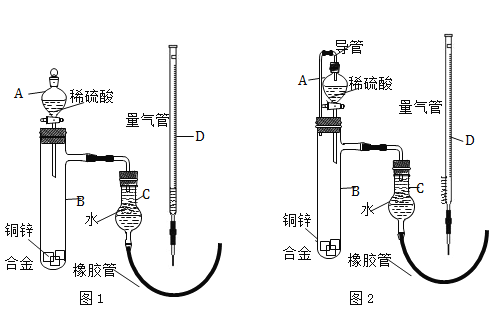
(5)小组同学交流发现上述方法测得的锌的质量分数会偏大,现将装置改为如图2所示,改进的目的是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)俄国化学家门捷列夫在总结前人经验的基础上,通过艰辛的努力,终于提出了现代元素周期表的雏形。下表为元素周期表的部分元素的相关信息,利用下表回答相关问题
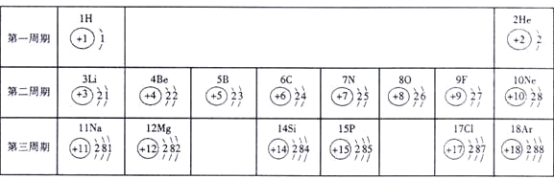
(1)请画出16号元素原子结构示意图 化学反应中该原子比较容易
(填“得到”或“失去”)电子变成离子;
(2)![]() 表示的是 (填离子符号);
表示的是 (填离子符号);
(3)上表中最活泼的金属元素与地壳中含量最多的元素组成的化合物是
(填化学式,任意填写一种);
(4)上表中第二、三周期元素最外层电子数的变化规律是___ _。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现欲探究一固体混合物A的成分,已知其中可能含有CuSO4、CaCO3、NH4NO3、Cu四种物质中的两种或多种。按下图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全反应)。
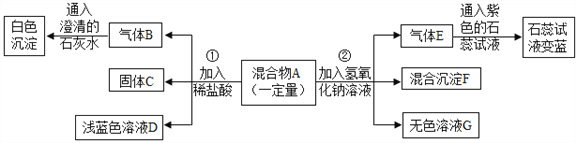
试根据实验过程和出现的现象做出判断,填写以下空白:
(1)气体E的气味是_____________________________。
(2)在混合物A中,共含有_____________种物质。
(3)固体C的化学式为_______________。
(4)溶液G中存在的金属阳离子为(写离子符号)_____________。
(5)写出实验过程①中所发生反应的化学方程式:________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B、C三种固体物质的溶解度曲线,试看图后回答:
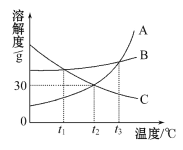
(1)在t3℃时,三种物质的溶解度的大小顺序是:______;
(2)在________时,B与C的溶解度相等;
(3)要从A、B、C的混合物中分离出A,最好用_______法;
(4)在温度介于t1℃和t2℃之间时,溶解相同质量的A、B、C,需要水的质量最小的是_____;
(5)t2℃时,将20 g A放入50 g水中充分溶解后,所得溶液质量是________g;
(6)我国北方有许多盐碱湖,湖水中溶有大量的氯化钠和纯碱(碳酸钠Na2CO3),那里的农民 “冬天捞碱,夏天晒盐”,其中“冬天捞碱”的道理是 __________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com