
分析 (1)考虑氧化铝其保护作用;考虑在生活中减少接触铝制品的方法分析;
(2)铁锈的主要成分是氧化铁;与水和氧气隔绝可以防止金属生锈;
(3)①考虑搅拌充分反应;②根据反应物、生成物,进行书写化学方程式;③考虑过滤操作中的仪器名称.
解答 解:(1)铝有较强的抗腐蚀性,其原因是常温下铝和氧气反应表面生成致密的氧化物薄膜,从而阻止铝进一步氧化;铝元素摄入过多会引起“老年痴呆症”,生活中要少用铝制餐具,或少吃用铝制易拉罐装的饮料、或少有铝箔包装食品等.
(2)铁生锈是铁与氧气、水分共同作用的结果,防止铁制品生锈的具体方法有涂油、刷漆;
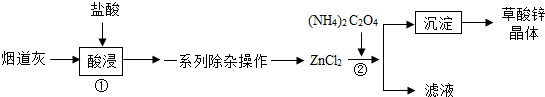
(3)①在酸浸操作过程中需不断搅拌,其作用是充分反应.
②经过系列除杂操作后,获得的溶液中主要成分为ZnCl2,加入(NH4)2C2O4后生成草酸锌晶体,故该反应的化学方程式ZnCl2+(NH4)2C2O4═ZnC2O4↓+2NH4Cl.
③上述流程中操作②名称为过滤,该过程中需要使用的玻璃仪器有漏斗、烧杯、玻璃棒.
故答案为:
(1)常温下铝和氧气反应表面生成致密的氧化物薄膜,从而阻止铝进一步氧化;生活中要少用铝制餐具,或少吃用铝制易拉罐装的饮料、或少有铝箔包装食品等.
(2)氧气、水分,涂油.
(3)①充分反应.②ZnCl2+(NH4)2C2O4═ZnC2O4↓+2NH4Cl.③过滤,漏斗.
点评 本题主要考查了金属的化学性质及其应用,了解常见金属的特性及其应用,并学会理论联系实际处理问题.


 习题精选系列答案
习题精选系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 化学式 | 颜色状态 | 酸碱性 | 加热 | 滴加稀盐酸 | 滴加硝酸银溶液 |
| NaCl | 白色固体 | 中性 | 受热不分解 | 无明显变化 | 生成白色沉淀 |
| NaNO2 | 白色固体 | 弱碱性 | 320℃以上分解生成刺激性气味的气体 | 生成红棕色气体 | 无明显变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
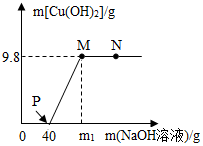 向含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH 溶液质量与生成沉淀质量关系如图,仅考虑沉淀为Cu(OH)2.则下列说法正确的是( )
向含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH 溶液质量与生成沉淀质量关系如图,仅考虑沉淀为Cu(OH)2.则下列说法正确的是( )| A. | P点溶液中的溶质只有一种 | |
| B. | N点时测得溶液pH>7 | |
| C. | 沉淀完全时,m1的数值为80 | |
| D. | M点溶液比P点溶液中氯化钠的质量分数小 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
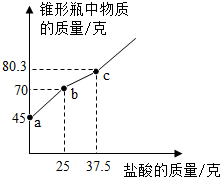 为测定某氢氧化钙(只含有碳酸钙杂质)样品的变质程度,称取研细的该样品12.4g放入锥形瓶中,加入32.6g水,充分振荡形成悬浊液,再向锥形瓶中逐滴滴加盐酸使其充分反应至无气泡产生,测得加入盐酸的质量与锥形瓶中物质的质量关系如图所示.
为测定某氢氧化钙(只含有碳酸钙杂质)样品的变质程度,称取研细的该样品12.4g放入锥形瓶中,加入32.6g水,充分振荡形成悬浊液,再向锥形瓶中逐滴滴加盐酸使其充分反应至无气泡产生,测得加入盐酸的质量与锥形瓶中物质的质量关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com