
 小学教材完全解读系列答案
小学教材完全解读系列答案科目:初中化学 来源:贵州省遵义市桐梓县2019届九年级下学期中考一模化学试卷 题型:单选题
化学与生产、生活、社会密切相关.下列说法中不正确的是( )
A. 使用“无磷洗涤剂”,促进水体富营养化
B. 研发易降解的塑料,防止白色污染
C. 回收处理工业废气,减少大气污染
D. 安装煤炭“固硫”装置,降低酸雨发生率
查看答案和解析>>
科目:初中化学 来源:山东省济南市2019届九年级下学期中考二模化学试卷 题型:单选题
下列化肥中,属于复合肥料的是( )
A. (NH4)2HPO4 B. K2SO4 C. NH4NO3 D. NH4Cl
查看答案和解析>>
科目:初中化学 来源:北京市朝阳区2019届九年级下学期中考一模化学试卷 题型:流程题
高纯氧化锌广泛应用于电子工业,某研究小组设计如下流程制备高纯氧化锌。
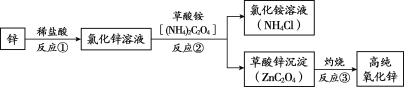
(1)反应①的基本反应类型为____________。
(2)反应③属于分解反应,除得到氧化锌外还生成2种气态氧化物,其化学式为_____________。
查看答案和解析>>
科目:初中化学 来源:北京市朝阳区2019届九年级下学期中考一模化学试卷 题型:单选题
用数轴表示某些化学知识直观、简明、易记。下列用数轴表示的化学知识,不正确的是
A. 生活中常见物质的pH:
B. 地壳中部分元素的含量:
C. 空气中部分成分的含量: 
D. 部分金属的活动性顺序:
查看答案和解析>>
科目:初中化学 来源:广东省广州市南沙区2019届九年级下学期学业水平综合测试化学试卷 题型:科学探究题
金属钴(Co)在国防工业中有重要应用。
(1)钴的化学性质与铁相似,与酸反应生成+2价的钴盐,CoCl2溶液为红色。
①请写出金属钴粉与稀盐酸反应的化学方程式:_____。
②预测上述反应发生的现象: _____。
③上述反应后新增的离子为: _____(填化学用语)。
(2)通过废锂电池(主要成份为LiCoO2、炭粉和铝箔)回收可得到草酸钴晶体。在实验室中研究不同条件下Co2+的浸出率(样品质量、加入盐酸体积均相同),结果如下表。从实验结果看,在仅考虑提高Co2+的浸出率的情况下,回答下列问题:
编号 | 温度/℃ | 时间/min | 盐酸浓度/% | 钴浸出率/% |
① | 80 | 120 | 10.5 | 90.82 |
② | 80 | 150 | 8.5 | 100.0 |
③ | 80 | 180 | 10.5 | 100.0 |
④ | 80 | 150 | 5.4 | 80.26 |
⑤ | 70 | 150 | 8.5 | 86.85 |
⑥ | 90 | 150 | 8.5 | 100.0 |
I.本实验研究了哪些因素对钴元素浸出率的影响:____。
II.实验⑤⑥的目的是______。
III.实验为最优反应条件______。
查看答案和解析>>
科目:初中化学 来源:广东省广州市南沙区2019届九年级下学期学业水平综合测试化学试卷 题型:填空题
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于棉纺、造纸业的漂白剂,也用于食品消毒、水处理等,亚氯酸钠受热易分解。
(1)亚氯酸钠(NaClO2)在酸性溶液中生成HClO2而发生分解,分解的化学方程式:5HClO2═4X↑+HCl+2H2O。HClO2读作____,其中氯元素的化合价为___;X的化学式___。
(2)以氯酸钠(NaClO3)等为原料可以制备亚氯酸钠。氯酸钠受热会分解,其生成物与氯酸钾分解的生成物相似。除此以外,氯酸钠与氯酸钾还具有一些其它相似的化学性质。
①试写出氯酸钠受热分解的化学方程式___。
②试分析氯酸钠与氯酸钾具有相似化学性质的原因___。(填字母)
A 都含氯元素 B 都含氧元素 C 都含ClO3- D 以上都是
查看答案和解析>>
科目:初中化学 来源:广东省广州市南沙区2019届九年级下学期学业水平综合测试化学试卷 题型:单选题
下图是锂原子结构示意图和锂元素在元素周期表中的相关信息。下列说法不正确的是( )
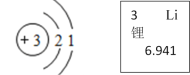
A. 锂元素属于金属元素
B. 锂原子核内有3个质子
C. 锂原子的相对原子质量是6.94l
D. 锂原子在化学反应中易得电子
查看答案和解析>>
科目:初中化学 来源:江苏省无锡市2019届九年级下学期学科质量抽测化学试卷 题型:流程题
绿矾被广泛用于医药和工业领域。工业上利用黄铜矿粉(含杂质)主要成分为CuFeS2制取绿矾(FeSO4·7H2O)的流程图如下
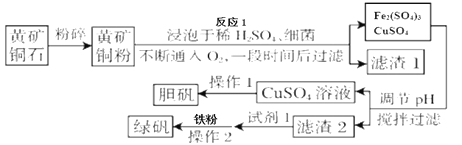
(相关资料)
①氢氧化亚铁不稳定,在空气中容易被氧气氧化成氢氧化铁。
②三价铁离子能和金属铁反应,方程式为:Fe2(SO4)3 + Fe = 3FeSO4
③FeSO4易溶于水但不溶于乙醇。
④部分阳离子以氢氧化物形式完全沉淀时溶液的pH见下表。
沉淀物 | 开始沉淀pH | 沉淀完全pH |
Cu(OH)2 | 4.2 | 6.7 |
Fe(OH)2 | 7.6 | 9.7 |
Fe(OH)3 | 1.5 | 2.8 |
(问题解答)
(1)将黄铜矿粉粹的目的是____________。
(2)在调节pH时,为了将滤渣2充分转化为沉淀而析出,需要调节溶液pH的范围为____________。在调节pH时常用铁的氧化物来调节,不选用NaOH溶液进行调节,理由是_______。
(3)最后得到的绿矾晶体用乙醇洗涤,不用水进行洗涤的目的是_______。
(4)黄铜矿粉能够在细菌作用下,与硫酸和氧气发生反应,请写出反应1的化学方程式_______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com