

| A. | 集气瓶破裂 | B. | 酸液飞溅 | C. | 测定结果偏大 | D. | 收集不满O2 |
分析 A、根据铁丝在氧气中燃烧的实验注意事项,进行分析判断.
B、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判断.
C、所选除氧剂要具备以下特征:本身能够在空气中燃烧;本身的状态为非气体;生成的物质为非气态.
D、根据实验室制取氧气的注意事项,进行分析判断.
解答 解:A、铁丝在O2中燃烧时,为防止生成物熔化溅落下来使瓶底炸裂,集气瓶的底部应放少量的水或铺一层细沙,图中集气瓶的底部没有放少量的水或铺一层细沙,可能会造成集气瓶破裂,故选项说法正确.
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;切不可把水注入浓硫酸中,这是因为浓硫酸的密度比水大,如果添加顺序颠倒,那么水会浮在水面上,又由于浓硫酸溶于水放出大量的热,能使水沸腾,容易造成酸液飞溅,故选项说法正确.
C、木炭在空气中燃烧生成二氧化碳气体或者一氧化碳气体甚至是两者的混合气体,虽除去氧气,而增加了新的气体,会造成测定结果偏小,故选项说法错误.
D、图中长颈漏斗的末端没有伸入液面以下,生成的氧气会从长颈漏斗中逸出,会导致收集不满氧气,故选项说法正确.
故选:C.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | 水是一种最常见的溶剂,自然界中的水都不是纯净物 | |
| B. | 酸雨的形成与大气中SO2等酸性污染物增多有关 | |
| C. | 水中N、P元素的增多会引起水体的富营养化污染,引起赤潮 | |
| D. | 纯碱水溶液,呈中性 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 等于5mL | B. | 小于5mL | C. | 大于5mL | D. | 无法判断 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 蒸发皿的质量(g) | 25.0 |
| 蒸发皿+食盐溶液(g) | 45.0 |
| 蒸发皿+食盐晶体(g) | 27.4 |
| 数据处理 | 溶液中溶质的质量分数为12%. |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 钢铁、铝合金、铜制品等是应用广泛的金属材料.据估计,每年全世界被腐蚀损耗的钢铁材料,约占全年钢产量的十分之一.某校化学兴趣小组的同学探究金属腐蚀的原因,设计如下实验:
钢铁、铝合金、铜制品等是应用广泛的金属材料.据估计,每年全世界被腐蚀损耗的钢铁材料,约占全年钢产量的十分之一.某校化学兴趣小组的同学探究金属腐蚀的原因,设计如下实验:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | MnO2固体中(KCl)---加入足量水,过滤、洗涤、干燥 | |
| B. | NaCl固体(K2CO3)---加入足量的稀盐酸,蒸发、结晶 | |
| C. | Fe粉(Al)---加入足量盐酸,蒸发、结晶 | |
| D. | CaCl2固体(CaCO3)---加入足量的稀盐酸、过滤、洗涤、干燥 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
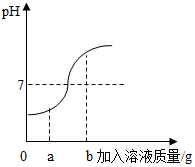 在用稀硫酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变
在用稀硫酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com