
分析 (1)根据质量守恒定律可知,反应前后减少的质量就是氢气的质量进行解答;
(2)根据生成的氢气的质量可以求出消耗硫酸的质量进行解答;
(3)根据氢气的质量可以求出参加反应锌的质量,即可求出铜的质量进而求出样品中铜的质量分数进行解答.
解答 解:(1)根据质量守恒定律可知,反应前后减少的质量就是氢气的质量,生成氢气的质量=10g+50g-59.9g=0.1g;故填:氢气;
(2)设参加反应锌的质量为x,消耗稀硫酸溶质的质量为y.
Zn+H2SO4=ZnSO4+H2↑
65 98 2
x y 0.1g
$\frac{65}{x}=\frac{98}{y}=\frac{2}{0.1g}$
x=3.25g
y=4.9g
铜的质量分数为:$\frac{10g-3.25g}{10g}$×100%=67.5%
答:样品中铜的质量分数为67.5%;
(3)19.6%的稀硫酸50g中溶质的质量=19.6%×50g=9.8g,所以稀硫酸有剩余,故反应后溶液中所含的溶质有生成的硫酸锌,还有剩余的硫酸;故填:H2SO4、ZnSO4.
点评 解答本题的关键是根据知道生成氢气质量,再根据氢气质量算出锌的质量,再计算铜的质量分数即可.


 作业辅导系列答案
作业辅导系列答案科目:初中化学 来源: 题型:解答题
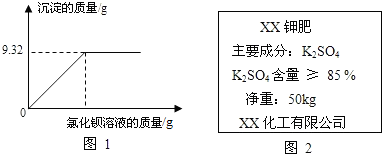
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 “碳海绵”具备高弹性的疏松多孔的结构,主要成分是石墨烯和碳纳米管(两者都是碳单质),对有机溶剂有超高、超快的吸附能力,而且只吸油不吸水.关于“碳海绵”的说法中不正确的是( )
“碳海绵”具备高弹性的疏松多孔的结构,主要成分是石墨烯和碳纳米管(两者都是碳单质),对有机溶剂有超高、超快的吸附能力,而且只吸油不吸水.关于“碳海绵”的说法中不正确的是( )| A. | 常温下“碳海绵”化学性质活泼 | |
| B. | “碳海绵”是一种混合物 | |
| C. | 可以用作处理海上漏油的新型吸油材料 | |
| D. | 在氧气中完全燃烧的产物是CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
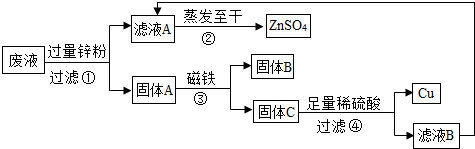
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )| A. | 甲的溶解度大于乙的溶解度 | |
| B. | t3℃时,将20 g乙加人50 g水中充分搅拌,可得到70 g溶液 | |
| C. | t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等 | |
| D. | 将t1℃甲、乙的饱和溶液各升温至t2℃,溶质质量分数相等 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
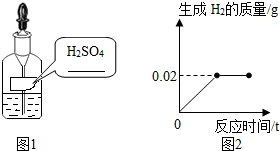 有一瓶标签破损的稀硫酸(如图1),为测定其溶质质量分数,取出7g该溶液,加入足量的锌粒,产生氢气的质量与反应时间关系如图2.请计算:该溶液中溶质的质量分数.
有一瓶标签破损的稀硫酸(如图1),为测定其溶质质量分数,取出7g该溶液,加入足量的锌粒,产生氢气的质量与反应时间关系如图2.请计算:该溶液中溶质的质量分数.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 20mL | B. | 小于20mL | C. | 大于20mL | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
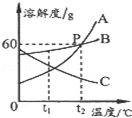 如图为A、B、C三种固体物质的溶解度曲线,根据图示完成问题:
如图为A、B、C三种固体物质的溶解度曲线,根据图示完成问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com