
【题目】“物质的组成与结构决定物质的性质”是化学科学中的重要观点。按照这一观点讨论下面的问题。
【1】酸溶液具有一些共同的化学性质,是因为酸溶液中都含有的离子是 ;碱溶液也具有一些共同的化学性质,是因为碱溶液中都含有的离子是 。
【2】写出下图所示的反应方程式 , 该反应前后,溶液中减少的离子是 。
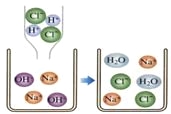
【3】100g20%的氢氧化钠溶液中含有氢氧化钠的质量是 g,与足量的稀盐酸反应,生成氯化钠的质量是 g。
【答案】
【1】氢离子(1分) 氢氧根(1分)
【2】NaOH+ HCl =NaCl+ H2O (2分) H+(氢离子)、OH-(氢氧根)(1分)
【3】20g(2分) 29.3g(或29.25g)(2分)
【解析】
(1)酸溶液中都含有氢离子,碱溶液中都含有的离子是氢氧根,(2)酸碱反应的实质就是氢离子和氢氧根离子反应生成水分子,所以溶液中减少的离子是H+(氢离子)、OH-(氢氧根),(3)溶质质量=溶液质量*溶质质量分数=100g*20%=20g,设与足量的稀盐酸反应,生成氯化钠的质量是X克,
NaOH+ HCl =NaCl+ H2O,
40
【1】5
20g X
40/
【2】5=20g/x,解得X=
【3】25g


科目:初中化学 来源: 题型:
【题目】化学实验小组的同学将足量锌粒加入一定量浓硫酸中,发现有大量气泡产生。他们对此气体的成分进行了探究。
(提出问题)锌粒加入该硫酸溶液反应生成的气体是什么?
(查阅资料)
①浓硫酸能与锌反应,但不产生氢气,也不会产生氧气,能生成二氧化硫气体;
②二氧化硫气体有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色。
(猜想与假设)
甲同学认为:气体可能是![]() ;
;
乙同学认为:气体可能是![]() ;
;
丙同学认为:气体还可能是_____。
(实验探究)
为了验证上述猜想,同学们在老师的指导下将产生的气体通过如下图的装置进行探究(部分夹持仪器略去)。
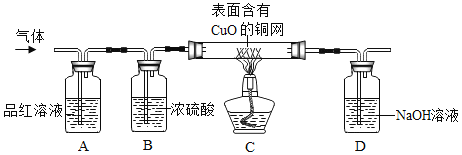
(1)实验开始后,观察到A中_____的现象,证明气体中含有![]() 。
。
(2)C装置先通一段时间气体后,再点燃酒精灯。一段时间后观察到玻璃管内_____的现象,证明气体中含有![]() 。
。
(3)D装置的作用是_____。
(实验结论)丙同学的猜想是正确的。
(反思与交流)
①锌和浓硫酸反应生成硫酸锌、水和二氧化硫,为什么反应过程中又产生了氢气呢?用文字简述原因:_____。
②锌与浓硫酸、稀硫酸反应都可以产生硫酸锌,如果需要制取硫酸锌,用锌与稀硫酸反应的优点是_____(任填一种合理的答案)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下图的溶解度曲线图回答:
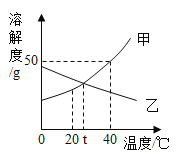
1.t℃时,甲、乙两物质的溶解度曲线相交于一点,说明________________________;
2.乙物质在不同温度下的溶解度变化趋势是:_______________________________;
3.40℃时,将60g甲物质溶解在100g水中,就可以得到______g甲物质的饱和溶液,此饱和溶液中溶质的质量分数为_______;
4.20℃时含有少量未溶解的乙物质的饱和溶液中,若要使乙物质完全溶解,可以采用的方法是_______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某反应的微观示意图。
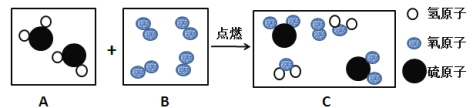
请回答:
(1)B框中的物质属于___________(填序号:①化合物、②单质、③纯净物、④混合物)。
(2)此反应的化学方程式为_____________________________,此图说明化学反应前后发生改变的微粒是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】测定石灰石中的碳酸钙的含量,取出2.5克石灰石样品,逐渐加入稀盐酸,充分反应后测得剩余固体质量与加入稀盐酸的质量关系如图所示.
(已知CaCO3+2HCl═CaCl2+H2O+CO2↑杂质不参与反应,也不溶于水)
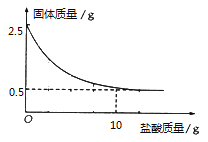
(1)石灰石样品中碳酸钙的质量是 g
(2)石灰石样品中碳酸钙的质量分数是
(3)计算稀盐酸溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】漫天飞舞的杨絮可能会引皮肤过敏,将赤霉酸(C19H22O6)注入杨树可以减少杨絮。下列有关“赤霉酸”的说法正确的是( )
A. 赤霉酸中碳元素的质量分数最高B. 赤霉酸由 47 个原子构成
C. 赤霉酸属于有机高分子化合物D. 赤霉酸中碳、氢元素的质量比为 19:22
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验小组同学为研究某公共场所铁制护栏锈蚀的程度,将 6.4g 已生锈的铁片,放入一浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如下图 所示(假设铁片除有 Fe2O3 外,不含其他杂质)。
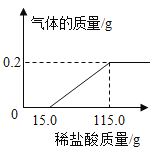
(1)生成氢气的质量为_____g。
(2)求稀盐酸中溶质的质量分数_______?求该铁片中 Fe2O3 的质量分数为多少_________?(写出计算过程,结果精确到到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】结合如图所示实验装置回答问题。
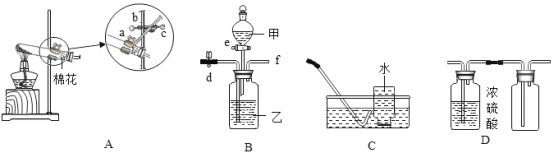
(1)装置AC组合制取氧气
①装置A中反应化学方程式为_____________,欲调整该装置中试管的倾斜角度,可调节旋钮________________(填”a”或”b”或”c”)。
②可用装置C收集氧气的原因是________。开始收集氧气的最佳时机是________________.
③实验结束撤装置时,发现试管破裂,可能的错误操作是________________(写一点)。
(2)装置B有多种功能
①装置B和D组合可制取干燥的气体:关闭止水夹d,打开活塞e,则该气体可能是________(填标号)。
X ![]() Y
Y ![]() Z
Z ![]()
②装置B可用来分离![]() 和
和![]() ,若试剂乙为氢氧化钠溶液,关闭活塞c,打开止水夹d,在导管口f处逸出的气体是________;接着关闭止水夹d,打开活塞e,滴加试剂甲,若甲为稀硫酸,又可收集到另一种气体,则该反应的化学方程式为______________
,若试剂乙为氢氧化钠溶液,关闭活塞c,打开止水夹d,在导管口f处逸出的气体是________;接着关闭止水夹d,打开活塞e,滴加试剂甲,若甲为稀硫酸,又可收集到另一种气体,则该反应的化学方程式为______________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属与生活息息相关,认识金属的性质对我们至关重要,认真阅读,回答问题。
材料一:镓(Ga)是灰蓝色或银白色的金属,熔点很低,沸点很高。其化学性质与铝相似,能与氧气在加热时反应。金属镓广泛应用于半导体材料,光电子工业和微波通讯工业等领域。镓的原子结构示意图如图所示。
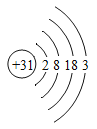
(1)镓的物理性质有_________________________。
(2)写出镓与氧气反应的化学方程式___________________________。
材料二:金属活动顺序在工农业生产和科学研究中有重要应用。现有铜、银、锌三种金属,某小组同学为了探究这三种金属的活动性,设计了以下实验:

(3)试管A中反应的化学方程式是_________________________,由实验A、B、C可推断出Ag、Zn、Cu三种金属的活动性由强到弱的顺序为_____________________。
(4)向C完全反应后的试管里加入一定质量的锌粒(如D试管)。D试管中一定会发生的反应是的化学方程式是________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com