
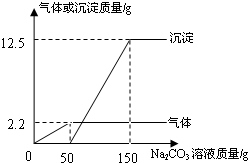
 在实验课上,同学们用锌和稀硫酸反应制取氢气.小明取反应后的溶液164.7g,滴入碳酸钠溶液,先后有气体和白色沉淀生成.加入碳酸钠溶液与生成沉淀或气体的质量关系如图.【已知Na2CO3+ZnSO4═ZnCO3↓+Na2SO4】
在实验课上,同学们用锌和稀硫酸反应制取氢气.小明取反应后的溶液164.7g,滴入碳酸钠溶液,先后有气体和白色沉淀生成.加入碳酸钠溶液与生成沉淀或气体的质量关系如图.【已知Na2CO3+ZnSO4═ZnCO3↓+Na2SO4】分析 (1)根据碳酸钠分别与硫酸反应生成二氧化碳、与硫酸锌反应生成碳酸锌沉淀分析;
(2)分别利用氢气的质量和沉淀的质量根据化学方程式计算出参加反应的碳酸钠的质量,再求和,进而求质量分数;
(3)分别利用氢气的质量和沉淀的质量根据化学方程式计算出生成的硫酸钠的质量,再求质量分数.
解答 解:(1)发生的反应有:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,Na2CO3+ZnSO4=ZnCO3↓+Na2SO4,则生成的气体是二氧化碳,沉淀为碳酸锌;
故答案为:CO2; ZnCO3
设硫酸反应消耗碳酸钠的质量为x,生成硫酸钠的质量为y;硫酸锌反应消耗碳酸钠的质量为m,生成硫酸钠的质量为n
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 142 44
x y 2.2g
$\frac{106}{x}=\frac{142}{y}=\frac{44}{2.2g}$
x=5.3g,y=7.1g
Na2CO3+ZnSO4=ZnCO3↓+Na2SO4
106 125 142
m 12.5g n
$\frac{106}{m}=\frac{125}{12.5g}=\frac{142}{n}$
m=10.6g,n=14.2g
(2)碳酸钠溶液中碳酸钠的质量分数为:$\frac{5.3g+10.6g}{150g}×100%$=10.6%
答:碳酸钠溶液中碳酸钠的质量分数为10.6%;
(3)反应后溶液的质量:164.7g+150g-2.2g-12.5g=300g
硫酸钠的质量分数:$\frac{7.1g+14.2g}{300g}$×100%=7.1%
答:所得溶液中硫酸钠的质量分数为7.1%.
答案:(1)CO2; ZnCO3;(2)10.6%;(3)答:所得溶液中硫酸钠的质量分数为7.1%.
点评 要明确该题中发生反应的过程,理清思路是解决该题的关键,有一定难度


科目:初中化学 来源: 题型:选择题
| A. | 揭开正在煮东西的锅盖时,会看到“白气”--气体的液化 | |
| B. | 铝制品耐腐蚀--铝的化学性质稳定 | |
| C. | 切菜的刀钝了要磨一磨--为了减小压强 | |
| D. | 煮粥时纯碱放多了加醋调节--发生了中和反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
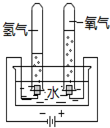 水的电解实验(实验装置如图)
水的电解实验(实验装置如图)查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
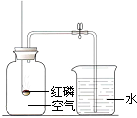 某同学用如图所示装置来测定空气中氧气的体积分数,请填写下列空白.
某同学用如图所示装置来测定空气中氧气的体积分数,请填写下列空白.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
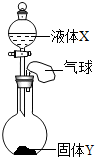 如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀.下列液体和固体组合符合题意的是( )
如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀.下列液体和固体组合符合题意的是( )| A. | 硝酸银溶液和氯化钠 | B. | 水和硝酸铵 | ||
| C. | 盐酸和硫酸钡 | D. | 过氧化氢溶液和二氧化锰 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 已知:A、B、C、D、E、F六种物质是初中化学常见的物质.A、B是单质,C、D、E都是氧化物.A、B、C转化为F的过程较为复杂,F的成份也较复杂.其主要成分是一种红色的固体.试根据各物质间的转化关系完成下列各题.(题中除反应条件未给出外,反应物和产物均已给出.)
已知:A、B、C、D、E、F六种物质是初中化学常见的物质.A、B是单质,C、D、E都是氧化物.A、B、C转化为F的过程较为复杂,F的成份也较复杂.其主要成分是一种红色的固体.试根据各物质间的转化关系完成下列各题.(题中除反应条件未给出外,反应物和产物均已给出.)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com