
分析 根据物质的性质进行分析,水是最常见的溶剂,石墨很软可用作铅笔芯,酒精具有特殊的香味,氢氧化钙是一种碱,可用于改良酸性土壤,小苏打是发酵粉的主要成分.
解答 解:(1)茅台酒的主要成分有的主要成分酒精,酒精具有特殊的香味;
(2)最常见的溶剂是水;
(3)石墨硬度比较小且常温下稳定,可用于制“2B”铅笔;
(4)缺乏维生素A会得夜盲症;
(5)熟石灰是一种碱,能与酸反应,可用来中和酸性土壤;
(6)小苏打是发酵粉的主要成分,用于烘焙糕点.
故答案为:(1)③;(2)①;(3)②;(4)⑥;(5)④;(6)⑤.
点评 本题考查了常见物质的用途,可以依据物质的性质进行判断,物质有多种性质,解答时应该理解物质的用途是由物质的哪种性质决定的.


科目:初中化学 来源: 题型:选择题
| A. | 碘酒是常用的消毒剂,其溶剂是碘 | |
| B. | 霉变的花生米洗净后仍可正常食用 | |
| C. | 可用结晶的方法提纯混有少量氯化钠的硝酸钾 | |
| D. | 汞、金、钛属于金属元素,硫、氮、铅属于非金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
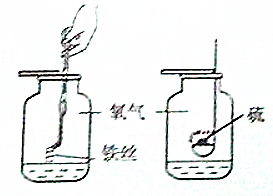 把下列物质中符合题目要求的序号填在横线上.
把下列物质中符合题目要求的序号填在横线上.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NH4HC03 | B. | KNO3 | C. | CO(NH2)2 | D. | K2S04 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
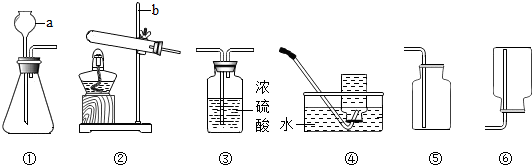
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
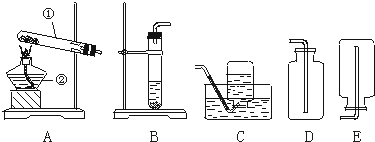
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
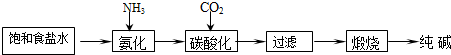
| 实验步骤 | 实验现象 | 实验结论 |
如图装置,把少量样品放入a试管中加热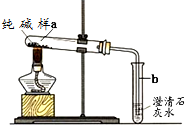 | b试管澄清石灰水 没变浑浊 | 纯碱样品中没有NaHCO3 |
| 取样品少量,溶解,加足量稀硝酸,再滴加硝酸银溶液 | 有白色沉淀产生 | 纯碱样品中有NaCl |
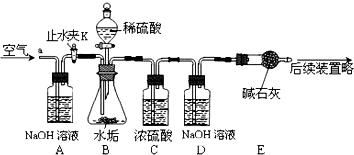
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com