
【题目】要配制100 g溶质质量分数为10%的氯化钠溶液,下列操作正确的是
A.将10g氯化钠固体直接放在天平的托盘上称量
B.将10g氯化钠固体放在天平右边的托盘上称量
C.为了加快氯化钠固体溶解,用温度计进行搅拌
D.配好的溶液倒入细口瓶中,盖紧瓶塞贴上标签
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】下列实验中,现象与结论对应关系正确的是( )
A | B | C | D | |
图 |
|
|
|
|
现 | 有大量气泡产生,生成的气体使澄清石灰水变浑浊 | 冷却后,打开弹簧夹,水被吸入瓶内,瓶内水面上升约 1/5 | ①中铁钉生锈, ②③中铁钉不生锈 | 滴加无色酚酞, 溶液呈红色,加入稀盐酸后红色变为无色 |
结论 | 该粉末中一定含有 | 氧气约占空气质量的1/5 | ①②对比说明铁生锈条件之一是要与水接触 | 反应后的溶液一定不呈 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】关注健康,预防疾病。下列叙述正确的是( )
A.锌是人体必需的微量元素,缺锌会影响生长发育,造成思维迟钝
B.每克油脂在人体内完全氧化,放出的能量比糖类多一倍以上,是重要的供能物质
C.缺乏维生素C,会引起夜盲症
D.人体口腔唾液中含有淀粉酶,它能将食物中的部分淀粉催化水解为葡萄糖
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3)来制取绿矾(FeSO4·7H2O),实现变废为宝,减少环境污染。简易流程如下: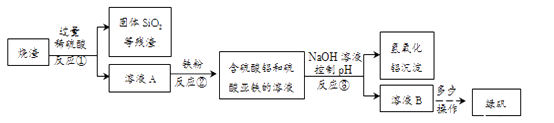
(1)反应①和反应③都要进行的操作是;
(2)写出反应②中发生反应的化学方程式为;
(3)用NaOH溶液控制pH的目的是。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验现象描述正确的是( )
A.硫在空气中燃烧发出明亮的蓝紫色火焰
B.电解水的实验中负极产生的气体使带火星的木条复燃
C.磷在空气中燃烧产生大量的白烟
D.生石灰加入一定体积的水,吸收大量的热
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】漂白粉的主要成分为次氯酸钙 [Ca(ClO)2] 和氯化钙,即可用作漂白剂,又可用作消毒剂。漂白粉中有效成分是 [Ca(ClO)2] ,漂白的原理是:Ca(ClO)2在空气中发生反应。Ca(ClO)2+ CO2+ H2O=CaCO3↓+ 2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色。
(1)HClO在常温下分解,反应为2HClO=2HCl+ O2↑。某瓶HClO溶液放置一段时间后,溶液的pH (填“增大”或“减小”或“不变”)。
(2)在漂白粉中滴加盐酸,能加快漂白的速率。写出漂白粉中加入盐酸反应的化学方程式。
(3)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验。
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3。
(4)【实验探究】限选试剂及仪器,盐酸、石灰水、品红溶液、试管、带导管的单孔塞。
实验操作 | 实验现象 | 实验结论 |
①取少量样品于试管中,。 | 有气体产生,气体使石灰水变浑浊。 | 猜想2成立 |
②在上述反应后试管中加少量。 | 。 |
(5)现有实验后的HCl与CaCl2的混合溶液,为了分析混合溶液中HCl和CaCl2的质量分数,设计了如下实验方案: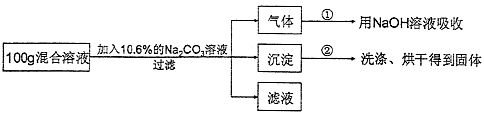
【实验数据】上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,共记录了两组实验数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.
根据实验设计及有关数据进行分析与计算:
m= .
(6)上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为多少?.(不考虑过滤中的损失,计算结果保留到小数点后一位.)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com