
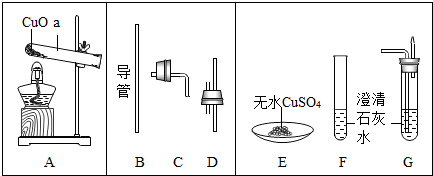
分析 根据一氧化碳还原氧化铜的反应特点选择仪器装置,因为加热前要先通入一氧化碳,反应后还要继续通入一氧化碳,因此要有排出气体并处理未反应的一氧化碳的装置;
反应前后仪器a中减小的质量即为氧化铜和碳反应生成二氧化碳的质量,根据二氧化碳质量可以计算碳的质量,进一步可以计算碳粉质量分数.
解答 解:①一氧化碳还原氧化铜时,除A装置外,还要选用通入气体和排出气体的装置,同时还有检验生成物和处理尾气的装置,符合要求的装置是DG.
故填:DG;导出CO2 和CO;检验CO2,处理CO.
②高温条件下,碳和氧化铜反应生成铜和二氧化碳,反应的化学方程式是:2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
故填:2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
③用碳和一氧化碳还原氧化铜的两个实验中,装置A中观察到的现象是:黑色固体逐渐变成红色.
故填:黑色固体逐渐变成红色.
④假设反应充分,称量准确,应选择Ⅰ组数据进行计算会更为合理准确,因为Ⅰ;Ⅱ中,反应生成的二氧化碳不能被全部吸收,导致计算结果不准确;
设碳的质量为z,
2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,
12 44
z xg
$\frac{12}{z}$=$\frac{44}{xg}$,
z=$\frac{12xg}{44}$,
碳粉质量分数为:$\frac{12xg_{44}}{mg}$×100%=$\frac{3x}{11m}$,
故填:Ⅰ;Ⅱ中,反应生成的二氧化碳不能被全部吸收;$\frac{3x}{11m}$.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 反应前后混合气体中氮气的质量分数不变 | |
| B. | 反应后气体混合物的组成有3种情况 | |
| C. | 若反应后气体是3种气体的混合物,则其中C、O元素的质量比一定小于12:16 | |
| D. | 若反应后气体中有氧气,则容器中C、O元素的质量比大于12:32 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com