
 CaO+CO2↑,属于分解反应.
CaO+CO2↑,属于分解反应. CaO+CO2↑;
CaO+CO2↑;

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:初中化学 来源: 题型:
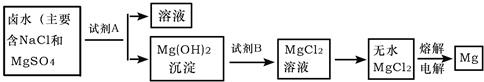
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2013年初中毕业升学考试(山东济南卷)化学(解析版) 题型:计算题
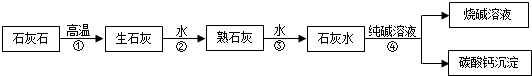
在工业上用纯碱和石灰石为原料制备烧碱,主要流程如图所示:
(1)在①﹣④四个过程中,发生了分解反应的是 (填序号).
(2)检验烧碱溶液中含有少量Na2CO3的具体方法是 .
(3)在室温下,将53g质量分数为10%的Na2CO3溶液与3000g澄清石灰水充分混合,恰好完全反应.则这时所得NaOH溶液的质量是多少?(计算结果精确至0.1g)
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com