
分析 【做出猜想】根据题意,乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时还生成一种白色固体,结合质量守恒定律,反应前后元素种类不变,进行分析解答.
【交流反思】根据氧化钙与水反应生成氢氧化钙,进行分析解答.
【进行实验】(一)剩余的猜想是碳酸钙和氢氧化钙,根据碳酸钙能与稀盐酸反应生成二氧化碳气体,进行分析解答.
(二)根据氢氧化钙溶液显碱性,进行分析解答.
由实验结论猜想三成立,则碳化钙(块状固体,化学式为CaC2)与水反应生成乙炔和氢氧化钙,进行分析解答.
解答 解:【做出猜想】乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时还生成一种白色固体,结合质量守恒定律,反应前后元素种类不变,白色固体是还可能是Ca(OH)2.
【交流反思】氧化钙与水反应生成氢氧化钙,故猜想一不成立.
【进行实验】(一)剩余的猜想是碳酸钙和氢氧化钙,碳酸钙能与稀盐酸反应生成二氧化碳气体,实验结论是猜想二不成立,则取少量白色固体于试管中,滴加稀盐酸,没有观察到有气泡产生.
(二)氢氧化钙溶液显碱性,取少量白色固体加入到水中,取上层清液,滴加无色酚酞溶液,溶液变红色,证明猜想三成立.
实验结论猜想三成立,则白色固体是氢氧化钙;碳化钙(块状固体,化学式为CaC2)与水反应生成乙炔和氢氧化钙,反应的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑.
故答案为:【做出猜想】Ca(OH)2;质量守恒定律;
【交流反思】CaO能与水反应;
【进行实验】(一)有气泡产生;(二)无色酚酞溶液;
结论:氢氧化钙;CaC2+2H2O=Ca(OH)2+C2H2↑.
点评 本题难度不大,明确实验目的、熟练掌握盐与碱的化学性质、质量守恒定律、氧化钙的化学性质等是正确解答本题的关键.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤渣中至少含有两种金属 | |
| B. | 反应后得到滤渣的质量一定大于反应前加入的镁粉的质量 | |
| C. | 向滤渣中加入一定量稀盐酸,可能有气体生成 | |
| D. | 滤液中一定含有硝酸镁 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
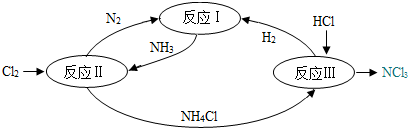
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

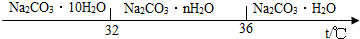

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
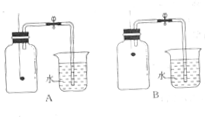
| 组 别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 进入集气瓶中水的体积(mL) | 20 | 21 | 19 | 21 | 22 | 18 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com