
【题目】某研究小组发现,维C泡腾片(保健药品,主要成分见图1),溶于水后有许多气泡产生(如图2).该小组同学进行如下探究。
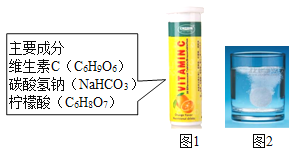
[提出问题]该气体的成分是什么?
该气体不可能含有SO2,因为________。
[提出猜想]Ⅰ.CO2 Ⅱ.__________。 Ⅲ.CO2和O2
[进行实验]
步骤 | 实验操作 | 实验现象 | 结论及化学方程式 |
(1) | 将气体通入________。 | _________。 | 该气体含有CO2,方程式是________。 |
(2) | 将带火星的木条伸入该气体中。 | 带火星的木条没有复燃。 | 该气体不是纯氧气。 |
[得出结论]该气体含有CO2_______(填“能”或“不能”)确定该气体中是否含氧气,理由是_________。
[讨论交流]维C泡腾片溶液是否呈酸性。向维C泡腾片溶液中滴加________试剂,溶液_______,说明该溶液显酸性。
【答案】根据质量守恒定律,反应物中不含硫元素(或化学反应前后元素种类不变) O2 澄清石灰水中 澄清石灰水变浑浊 CO2+Ca(OH)2=CaCO3↓+H2O 不能 因为气体中含有CO2相对较多时,带火星的木条也不能复燃(合理即可) 紫色石蕊 溶液由紫变成红色(合理即可)
【解析】
[提出问题]如图可知,反应前的物质不含有硫元素,所以反应后的物质,也不含有硫元素,所以反应后不含有SO2。故答案为根据质量守恒定律,反应物中不含硫元素(或化学反应前后元素种类不变)。
[提出猜想]II.由题干的猜想可知,该猜想是O2
[进行实验]步骤(1)用于检验CO2,所以应该在实验操作中,将气体通入澄清石灰水,澄清石灰水变浑浊,化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O
[得出结论]气体含有CO2时,CO2量小O2量大时,带火星的木条可复燃,但是O2量小CO2量大时,带火星的木条不能复燃,所以带火星的木条复燃的条件是含有氧气且氧气的浓度到达一定程度.
[讨论交流]紫色石蕊试剂可以检验溶液的酸碱性,所以可以滴加紫色石蕊试剂,紫色石蕊遇酸变红.


科目:初中化学 来源: 题型:
【题目】某兴趣小组的同学欲鉴别稀硫酸、硫酸钠和氢氧化钠三种无色溶液,他们把标有序号的三种无色溶液分别滴入标有对应序号的三支试管中,向三支试管中分别滴加无色酚酞试液,如图甲所示,鉴别出1号溶液。然后向2号、3号试管中分别加入少量已经变红的1号溶液,现象如图乙所示。请回答:
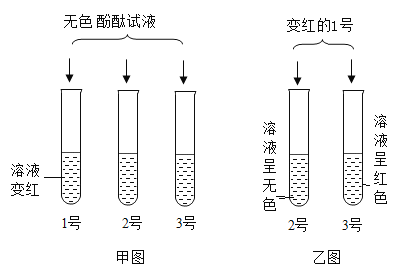
(1)甲图1号试管中是_____溶液。
(2)乙图2号试管中发生化学反应的微观实质是_____。
(提出问题)乙图2号试管反应后溶液中溶质的成分是什么?
(猜想假设)猜想一:Na2SO4;猜想二:_____(填化学式)。
(进行实验)取少量乙图2号试管中反应后的溶液于另一试管中,向其中加入_____(填试剂名称,观察到_____观象,证明猜想二正确。
(交流拓展)实验结束后,将所有废液倒入同一废液缸中,溶液呈红色,要将该废液调至中性后排放,可向废液中加入适量_____(填字母序号)
A 稀盐酸 B 熟石灰 C 石灰石
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请参与探究金属铝和铜的活动性强弱,完成下列内容。
[设计实验]
编号 | 操作 | 现象 | 解释 |
甲 | 将表面未打磨的铝丝浸入CuSO4溶液中 | 无明显现象 | |
乙 | 将表面打磨后的铝丝浸入CuSO4溶液中 | 铝丝表面析出红色固体 | 化学方程式为:____________, |
丙 | 将表面未打磨的铝丝浸入CuCl2溶液中 | 铝丝表面析出__________色固体 |
|
(1)铝丝表面有一层氧化膜,其形成的原因是(用化学方程式表示)________________。
(2)比较实验乙和实验________________(填“甲”或“丙”)可得知:打磨能破坏氧化铝薄膜。
[结论与反思]
(1)据此可知金属活动性Al比Cu_______________(填“强”或 “弱”)。
(2)查阅资料得知: CuSO4 溶液中有Cu2+、SO42-、H2O三种粒子,CuCl2溶液中有Cu2+、CI-、H2O三种粒子。小明同学对实验丙的现象进行分析,你认为合理的猜想是______________。
AH2O 破坏了氧化铝薄膜
BCl- 破坏了氧化铝薄膜
CCu2+ 破坏了氧化铝薄膜
DSO42-破坏了氧化铝薄膜
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将质量相等,表面积相同的锌片和镁片分别加入到完全相同的两份稀盐酸中,反应速率随时间变化的关系如图所示,反应后两种金属都有剩余,下列说法错误的是
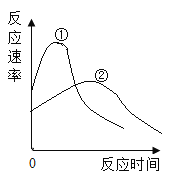
A.曲线②表示的是锌与稀盐酸反应速率的变化
B.两种金属和稀盐酸反应最终产生的氢气质量相等
C.镁和稀盐酸反应速率快是因为镁的相对原子质量小
D.刚开始时反应速率都变快是因为反应放热
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室以某石灰石(含少量Fe2O3)为原料制备高纯CaCO3的步骤如下:
溶解 向石灰石样品中加入适量盐酸,至反应完全。
除铁 加入氨水调节pH,然后加入适量Ca(OH)2,充分反应后过滤。
沉淀 向滤液中补充氨水,通入CO2,反应一段时间。
分离 过滤、洗涤、干燥得高纯CaCO3
(1)溶解时,CaCO3与盐酸反应的化学方程式为_______。判断样品已完全反应的实验现象是_______。
(2)除铁时,选用Ca(OH)2而不选用NaOH,其主要原因是Ca(OH)2价格低且来源广、__________、__________;过滤所得滤渣主要成分为___________。
(3)沉淀时,其他条件相同,反应温度对CaCO3产率的影响如图。高于35℃时,CaCO3产率下降的主要原因是__________。
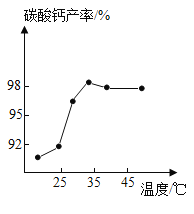
(已知:产率=![]() ×100%)
×100%)
(4)分离时,若向过滤所得滤液中加入________(填化学式)并加热,则可回收NH3。
(5)该实验可以循环利用的物质有H2O和________。
(6)石灰厂煅烧石灰石生产CaO,若要得到28tCaO,则至少需要含CaCO390%的石灰石多少吨________?(写出计算过程,保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】丁基锂(C4H9Li)是橡胶合成工业中一种常用的试剂。白色粉末,熔点-95℃,沸点80℃,遇水、空气均易自燃。下列关于丁基锂的说法正确的是
A. 丁基锂是由4个碳原子、9个氢原子、1个锂原子构成的
B. 丁基锂中碳元素质量分数为75%
C. 丁基锂运输或使用过程中如果发生燃烧,可以用水浇灭
D. 丁基锂是有机高分子化合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019年12月17日下午,我国首艘国产航母“山东舰”正式交付海军服役。建造航母需要大量的金属钛。工业上以钛铁矿(主要成分为钛酸亚铁FeTiO3)为原料生产钛。下图为钛元素在元素周期表中的信息和其原子结构示意图。回答下列问题:
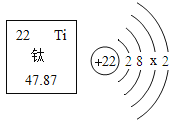
(1)钛原子核外有几个电子层________,钛元素属于______元素(填“金属”或“非金属”)。
(2)钛铁矿属于_______(填字母序号)。
A单质 B化合物 C纯净物 D混合物
(3)钛酸亚铁FeTiO3中钛的化合价________。
(4)对图中钛原子的信息解读不正确的是________。
A图中X的数值为10 B在化学反应中,钛原子容易失去电子
C核内质子数为22 D相对原子质量为47.87g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学校的化学兴趣小组为了测定一份石灰石样品的纯度,取出2.5g石灰石样品(样品中杂质不溶于水,且不参与反应)并粉碎,然后逐渐加入稀盐酸,充分反应后剩余固体与加入稀盐酸的质量关系如图所示。

(1)石灰石样品粉碎的目的是______。
(2)石灰石样品的纯度是______。
(3)求生成的二氧化碳气体的质量_____(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种物质的溶解度曲线如下图所示,请根据图回答下列问题:
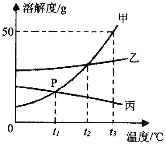
⑴P点表示的含义是________________。
⑵t2℃时,将丙物质的不饱和溶液变成饱和溶液,在不改变溶质质量分数的前提下,可采取的方法________________。
⑶t3℃时,将甲和乙两种物质的饱和溶液各100g分别蒸发10g水,然后降温到t2℃,所得溶液中溶质质量关系是甲________________乙(填“>”、“<”或“=”)。
⑷下列说法正确的是________________(填字母序号)。
A t2℃时,甲、乙两种物质的溶液溶质质量分数一定相等
B t3℃时,配制300g甲的饱和溶液,需要固体甲的质量为100g
C t3℃时,甲、乙两种物质的饱和溶液降温到t1℃,甲析出的晶体一定比乙多
D t1℃时,将等质量的甲、乙、丙三种物质制成该温度下的饱和溶液,所需溶剂的质量甲=丙>乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com