
 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:初中化学 来源: 题型:
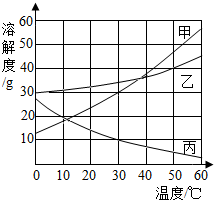 (2012?和平区二模)甲、乙、丙三种固体物质的溶解度曲线如图所示.
(2012?和平区二模)甲、乙、丙三种固体物质的溶解度曲线如图所示.查看答案和解析>>
科目:初中化学 来源:2011-2012学年贵州省九年级下学期模拟考试化学试卷三(解析版) 题型:填空题
下表列出了两种固体物质的溶解度,回答下列问题:
|


|
0oC |
10 oC |
20 oC |
30 oC |
40 oC |
||||||||||||||
|
A |
37.4g |
36.0g |
34.7 g |
33.8 g |
33.2 g |
||||||||||||||
|
B |
13.3 g |
20.9 g |
31.6 g |
45.8 g |
63.9 g |
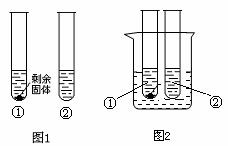
(1)10℃时,取A、B两种固体各3.5g,分别放入10g水中充分溶解,有如图1所示的实验现象,

试管①中溶解的物质是 (填“A”或“B”),其溶液中溶质的质量分数为 (精确到0.1%)。将两只试管同时放入盛有水的烧杯中(如图2),
向烧杯中加入足量NaOH固体并轻轻搅拌,观察到两个试管中的现象分别是:
试管① ;
试管② 。
(2)若向烧杯中加入适量下列物质,两试管中的现象与加NaOH固体相同是 。
A.冰 B.氯化钠 C.生石灰 D.硝酸铵
查看答案和解析>>
科目:初中化学 来源: 题型:
下表列出了两种固体物质的溶解度,回答下列问题:
|
| 0oC | 10 oC | 20 oC | 30 oC | 40 oC | ||||||||||||||
| A | 37.4g | 36.0g | 34.7 g | 33.8 g | 33.2 g | ||||||||||||||
| B | 13.3 g | 20.9 g | 31.6 g | 45.8 g | 63.9 g |
(1)B为硝酸钾,硝酸钾溶液中的溶剂是 。
(2)将硝酸钾的不饱和溶液变为饱和溶液的方法有 。
(3)10 oC时,取A、B两种固体各35g,分别放入100g水中充分溶解,有如图所示的实验现象,
试管①中溶解的物质是 (填“A”或“B”),其溶液中溶质的质量分数为 (保留一位小数),将两只试管分别放入盛有水的烧杯中(图2),向烧杯中加入足量NaOH并轻轻搅拌,观察到
。
(4)若向烧杯中加入适量下列物质,两试管中的现象与加NaOH不同的是
 A.冰 B.干冰 C.生石灰 D.硝酸铵
A.冰 B.干冰 C.生石灰 D.硝酸铵
查看答案和解析>>
科目:初中化学 来源: 题型:
下表列出了两种固体物质的溶解度,回答下列问题:
|

| 0oC | 10 | 20 oC | 30 oC | 40 oC | ||||||||||||||
| A | 37.4g | 36.0g | 34.7 g | 33.8 g | 33.2 g | ||||||||||||||
| B | 13.3 g | 20.9 g | 31.6 g | 45.8 g | 63.9 g |
(1)10℃时,取A、B两种固体各3.5g,分别放入10g水
中充分溶解,有如图1所示的实验现象,试管①中溶解的
物质是 (填“A”或“B”),其溶液中溶质的质
量分数为 (精确到0.1%)。将两只试管同时放入盛有水的烧杯中(如图2),
向烧杯中加入足量NaOH固体并轻轻搅拌,观察到两个试管中的现象分别是:
试管① ![]()
![]() ;
;
试管② 。
(2)若向烧杯中加入适量下列物质,两试管中的现象与加NaOH固体相同是 。
A.冰 B.氯化钠 C.生石灰 ![]()
![]() D.硝酸铵
D.硝酸铵

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
某实验小组利用废硫酸液制备K2SO4并研究CaSO4•2H2O加热分解的产物。
 一、K2SO4的制备
一、K2SO4的制备
(1)将CaCO3研成粉末的目的是 ▲ 。
(2)上述流程中可循环使用的物质有CO2和 ▲ (填写化学式)。
(3)反应Ⅲ中相关物质的溶解度如下表。你认为反应Ⅲ在常温下能实现的原因是 ▲ 。
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(4)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是 ▲ ;为检验此晶体是否洗涤干净,可取最后 一次洗涤液,先加入 ▲ (选填序号,下同),振荡、静置,再向上层清液中滴加 ▲ ,观察现象即可判断。
一次洗涤液,先加入 ▲ (选填序号,下同),振荡、静置,再向上层清液中滴加 ▲ ,观察现象即可判断。
a.AgNO3溶液 b.过量的BaCl2溶液 c.过量的Ba(NO3)2溶液
(5)分离所得的CaSO4•2H2O含有CaCO3,可用盐酸除去,该的化学反应方程式 ▲ 。
 (6)为了测定CaSO4•2H2O和CaCO3的质量比x:y,实验小组利用下图所示的装置(夹持仪器省略)进行实验。
(6)为了测定CaSO4•2H2O和CaCO3的质量比x:y,实验小组利用下图所示的装置(夹持仪器省略)进行实验。

 |
|
①实验前首先要 ▲ ,再装入样品。装置A的作用是 ▲ 。
②已知CaSO4•2H2O在160℃生成CaSO4,1350℃时CaSO4开始分解;CaCO3在900℃时分解完全。现控制B装置温度900℃进行实验并采集了如下数据:
a.反应前玻璃管与样品的质量m1g b.反应后玻璃管中固体的质量为m2g
c.装置C实验后增重m3g d.装置D实验后增重m4g

 某同学选用b、d或c、d数据组合求出x:y的值,若无装置E,则实验测定结果将 ▲ (填“偏大”、“偏小”或“无影响”)。你认为还可选用上述的 ▲
某同学选用b、d或c、d数据组合求出x:y的值,若无装置E,则实验测定结果将 ▲ (填“偏大”、“偏小”或“无影响”)。你认为还可选用上述的 ▲  (选填序号)两个数据组合也可求出x:y的值。
(选填序号)两个数据组合也可求出x:y的值。
(7)CaSO4•2H2O受热会逐步失去结晶水。取纯
净CaSO4•2H2O固体3.44g,放在(5)的实
验装置B中进行加热,测定固体质量随温
度的变化情况如右图所示。
①G点固体的化学式是 ▲ 。
②将T2~1400℃温度段加热固体所产 生的
生的
气体
|
则H~I段发生反应的化学方程式为 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com