





科目:初中化学 来源: 题型:阅读理解
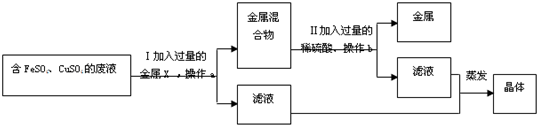
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
| KCl | CaCl2 | NaCl | MgCl2 | A1C13 | ZnCl2 ZnCl2 |
FeCl2 FeCl2 |
CuCl2 CuCl2 |


查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 某学习小组的同学对物质燃烧知识进行了整理和探究.请你一起参与!
某学习小组的同学对物质燃烧知识进行了整理和探究.请你一起参与!
| ||
| ||
| 物质名称 | 物质状态 | 沸点(℃) | 燃烧达到的温度(℃) | 是否产生火焰 |
| 氢气 | 气 | -259 | 约2750 | 是 |
| 一氧化碳 | 气 | 约-190 | 约2500 | 是 |
| 木炭 | 固 | 约4827 | 约1200 | 否 |
| 石蜡 | 固 | 约300 | 约600 | 是 |
| 钠 | 固 | 约883 | 约1400 | 是 |
| 铁 | 固 | 约2750 | 约1800 | 否 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某学习小组的同学对物质燃烧知识进行了整理和探究.请你一起参与!
某学习小组的同学对物质燃烧知识进行了整理和探究.请你一起参与!| 物质名称 | 物质状态 | 沸点(℃) | 燃烧达到的温度(℃) | 是否产生火焰 |
| 氢气 | 气 | -259 | 约2750 | 是 |
| 一氧化碳 | 气 | 约-190 | 约2500 | 是 |
| 木炭 | 固 | 约4827 | 约1200 | 否 |
| 石蜡 | 固 | 约300 | 约600 | 是 |
| 钠 | 固 | 约883 | 约1400 | 是 |
| 铁 | 固 | 约2750 | 约1800 | 否 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com