
| A、过滤时,倾倒液体用玻璃棒引流 |
| B、用剩的药品放回原瓶 |
| C、用细口瓶盛放固体药品 |
| D、用托盘天平称量药品时,左盘放砝码,右盘放药品 |
科目:初中化学 来源: 题型:
| 作物 | 茶 | 油菜 | 西瓜 | 甘草 |
| 适宜pH | 4.5-5.5 | 6.9-7.1 | 7.0-7.5 | 7.2-8.5 |
| A、茶 | B、油菜 | C、西瓜 | D、甘草 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 物 质 | X | Y | Z | Q |
| 反应前质量(g) | 4 | 10 | 1 | 21 |
| 反应后质量(g) | 0 | 12 | 15 | 待 测 |
| A、反应后生成15g Z |
| B、反应中Y与Q发生改变的质量之比1:1 |
| C、该反应方程式中X与Q的化学计量数之比为2:5 |
| D、反应后Q的质量为9g |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、植物的光合作用,矿石粉碎 |
| B、碘升华,红磷燃烧 |
| C、食物腐烂,铁生锈 |
| D、海水经日晒后析出食盐晶体,分离液态空气法制氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:
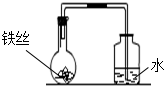 某同学用A、B、C三个烧瓶分别按图所示的实验装置进行实验,每隔一段时间测量导管中水面上升的高度(设环境温度和压强保持不变),结果如下表(表中所列数据为导管中水面上升的高度/cm):
某同学用A、B、C三个烧瓶分别按图所示的实验装置进行实验,每隔一段时间测量导管中水面上升的高度(设环境温度和压强保持不变),结果如下表(表中所列数据为导管中水面上升的高度/cm):| 时间/天 | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| A瓶(干燥的铁丝) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| B瓶(沾了食盐水的铁丝) | 0 | 0.4 | 1.2 | 3.4 | 5.6 | 7.6 | 9.8 |
| C瓶(沾了清水的铁丝) | 0 | 0 | 0 | 0.3 | 0.8 | 2.0 | 3.5 |
| D瓶(完全浸没在食盐水中的铁丝) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
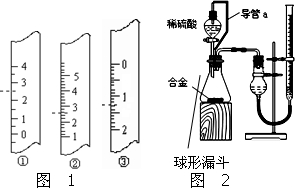 铝镁合金已成为飞机制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
铝镁合金已成为飞机制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com