
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案科目:初中化学 来源:2012-2013学年云南省驿镇二中九年级上学期12月月考化学试卷(带解析) 题型:计算题
(本小题共6分,其中⑴题2分,⑵题4分)
某化学兴趣小组为了测定某种生铁样品中铁的质量分数,在实验室将5.8g生铁样品放入烧杯中,加入50g稀硫酸恰好完全反应(杂质不参加反应),反应后称得剩余物质的总质量为55.6g。请回答:
⑴你分析后一定能计算出产生氢气的质量为 。你上述计算的理论依据是 。
⑵请你参与这个小组,来计算出该生铁样品中铁的质量分数是多少?(结果保留一位小数)
查看答案和解析>>
科目:初中化学 来源:2011届北京市大兴区中考二模化学试卷(带解析) 题型:探究题
(6分)某化学兴趣小组的同学对食品保鲜袋进行了如下研究。
【研究课题】食品保鲜袋的元素组成。
【查阅资料】碱石灰是由NaOH和CaO组成的吸湿剂;无水硫酸铜可作吸水剂,且吸水后由白色变为蓝色。
【提出猜想】保鲜袋可能由“碳、氢、氧”中的两种或三种元素组成。
【实验设计】小组同学设计了如下实验装置,利用燃烧法测定保鲜袋的元素组成。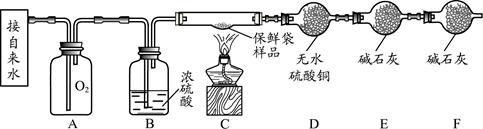
【实验步骤】
(1)按上图图示连接好仪器。
(2)检查装置的气密性。
(3)按图示装好药品和1.4g剪碎的保鲜袋样品,除D、E、F外将仪器按原图组装。
(4)向A中缓慢注水一段时间后,将已称重的D、E两干燥管和未称重的F干燥管接到C的尾端。
(5)点燃C处的酒精灯,直至保鲜袋子碎片完全燃烧。
(6)熄灭酒精灯并继续向A中注水一段时间。
(7)分别对D、E进行第2次称重。
【实验分析】
(1)B处的浓硫酸的作用是 。F处干燥管的作用是 。
(2)在点燃酒精灯前,要向A中缓慢注水一段时间是为了 。
(3)熄灭酒精灯后继续向A中注水一段时间是为了 。
【实验结论】第1次对D、E称重质量分别为(此处缺少数据);第2次对D、E称重质量分别为(此处缺少数据),则该食品保鲜袋的元素组成为 。(本小题无法解答)
查看答案和解析>>
科目:初中化学 来源:2010-2011学年北京市大兴区中考二模化学试卷(解析版) 题型:探究题
(6分)某化学兴趣小组的同学对食品保鲜袋进行了如下研究。
【研究课题】食品保鲜袋的元素组成。
【查阅资料】碱石灰是由NaOH和CaO组成的吸湿剂;无水硫酸铜可作吸水剂,且吸水后由白色变为蓝色。
【提出猜想】保鲜袋可能由“碳、氢、氧”中的两种或三种元素组成。
【实验设计】小组同学设计了如下实验装置,利用燃烧法测定保鲜袋的元素组成。
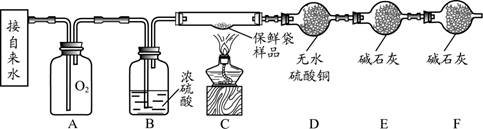
【实验步骤】
(1)按上图图示连接好仪器。
(2)检查装置的气密性。
(3)按图示装好药品和1.4g剪碎的保鲜袋样品,除D、E、F外将仪器按原图组装。
(4)向A中缓慢注水一段时间后,将已称重的D、E两干燥管和未称重的F干燥管接到C的尾端。
(5)点燃C处的酒精灯,直至保鲜袋子碎片完全燃烧。
(6)熄灭酒精灯并继续向A中注水一段时间。
(7)分别对D、E进行第2次称重。
【实验分析】
(1)B处的浓硫酸的作用是 。F处干燥管的作用是 。
(2)在点燃酒精灯前,要向A中缓慢注水一段时间是为了 。
(3)熄灭酒精灯后继续向A中注水一段时间是为了 。
【实验结论】第1次对D、E称重质量分别为(此处缺少数据);第2次对D、E称重质量分别为(此处缺少数据),则该食品保鲜袋的元素组成为 。(本小题无法解答)
查看答案和解析>>
科目:初中化学 来源:2012-2013学年云南省九年级上学期12月月考化学试卷(解析版) 题型:计算题
(本小题共6分,其中⑴题2分,⑵题4分)
某化学兴趣小组为了测定某种生铁样品中铁的质量分数,在实验室将5.8g生铁样品放入烧杯中,加入50g稀硫酸恰好完全反应(杂质不参加反应),反应后称得剩余物质的总质量为55.6g 。请回答:
⑴你分析后一定能计算出产生氢气的质量为 。你上述计算的理论依据是 。
⑵请你参与这个小组,来计算出该生铁样品中铁的质量分数是多少?(结果保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
根据下图回答问题。
 |
(1)仪器a的名称是 。
(2)实验室制取二氧化碳所选用的发生装置是 (填装置序号,下同),不选择装置E收集二氧化碳的原因是______________________。
(3)实验室用高锰酸钾制取氧气反应的化学方程式是 _____________________ ,
所选用的收集装置是E或 。主要的实验步骤有:①加热 ②装药品并固定
试管 ③检查装置的气密性 ④用排水法收集氧气 ⑤停止加热 ⑥将导管从水
槽中取出。正确的操作顺序是 _____________ (用序号表示)。
(1)酒精灯(2)B 二氧化碳能溶于水且与水反应(只答一点给分)
|
32.(5分)32.(5分)某化学小组测定空气中氧气的体积分数。
 (1)根据右图回答问题。
(1)根据右图回答问题。
①红磷燃烧的化学方程式为__________________________________。
②若将红磷改为木炭,反应结束后降至室温,打开止水夹,烧杯
中的水不倒吸入集气瓶的原因是______________________________
 _______________________________________________。
_______________________________________________。
(2)用四硫化钠(Na2S4)固体可替代红磷测定空气中氧气的体积分数。
反应原理为:2Na2S4+O2+2H2O 8S↓+4NaOH(氢氧化钠)。
小资料:四硫化钠(Na2S4)与氧气、水反应生成难溶于水的固体硫(S)和易溶于水
的氢氧化钠。
【实验过程】
①取足量的四硫化钠固体加入试管中,再加入适量的水,迅速塞紧橡胶塞,充分振荡。测量液面至橡胶塞下沿的距离,记录数据h1(如图1所示)。
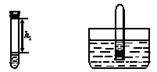
图1 图2
②将该试管插入水中(如图2所示),拔下橡胶塞,观察到__________,塞紧橡胶塞。将试管取出,倒转过来,测量液面至橡胶塞下沿的距离,记录数据h2。理论上h2∶h1= 。
③按照①和② 再重复实验2次。3次实验数据如下表所示。
再重复实验2次。3次实验数据如下表所示。
| 第1次 | 第2次 | 第3次 | |
| h1/cm | 11.0 | 11.4 | 11.6 |
| h2/cm | 8.7 | 9.1 | 9.2 |
根据第3次实验数据,计算空气中氧气的体积分数为 %(结果精确到 0.1%)。
(1)①4P + 5O 2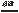 2P2O5
2P2O5
② 因为木炭燃烧生成二氧化碳气体,集气瓶内气体体积不变,瓶内气体压强没有明显变
因为木炭燃烧生成二氧化碳气体,集气瓶内气体体积不变,瓶内气体压强没有明显变
化,所以,当打开止水夹时水不会吸入到集气瓶中。
(2)②试管内液面上升至液面高度不再改变 79∶100(或4∶5)  ③ 20.7
③ 20.7
33.(8分)某兴趣小组同学阅读课外资料得知:很多因素都能影响过氧化氢分解速度。于是,
同学们探究影响过氧化氢分解速度的某种因素。
【实验过程】实验数据记录如下:
| 过氧化氢溶液的质量 | 过氧化氢溶液的浓度 | MnO2的质量 | 测量数据 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9 mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16 mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31 mL |
【实验分析】
(1)过氧化氢分解的化学方程式为______________________________________。
(2)表格中的“测量数据”的指的是:相同时间内_________________________________。
(3)本实验中,测量O2体积的装置是________(填编号)。
 |
【实验结论】
在相同条件下______________________________________________。
【交流评价】
(1)甲同学提出在上述实验中测量______________同样能得出相同的结论。
 (2)乙同学提出用右图装置进行实验,通过比较_____________
(2)乙同学提出用右图装置进行实验,通过比较_____________
___________________也能达到实验目的。
【实验反思】
除了上述因素会影响过氧化氢分解速度外, ___________(写
一种)也会影响过氧化氢分解速度,你的实验方案是______________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com