
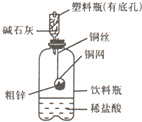
 某化学兴趣小组拟用右图装置对某粗锌样品进行纯度检测.请填写以下实验报告.
某化学兴趣小组拟用右图装置对某粗锌样品进行纯度检测.请填写以下实验报告.| 65 |
| X |
| 2 |
| 0.2克 |
| 6.5 |
| 10 |


科目:初中化学 来源: 题型:
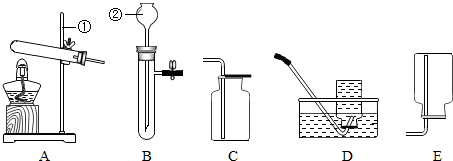
| A、每取用一种药品后,都应盖好试剂瓶,标签朝外,放回原处 |
| B、若取用无腐蚀性的药品,可以用手直接拿 |
| C、用胶头滴管滴加液体时,应将滴管伸入试管中 |
| D、用药匙将粉末药品撒入试管中 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、大于20mL |
| B、等于20mL |
| C、小于20mL |
| D、无法判断 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
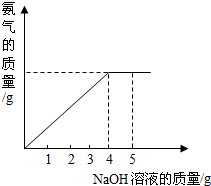 硝酸铵是农业生产中常用的化学肥料.为测定某含有少量NaNO3的硝酸铵样品中NH4NO3的纯度,取 2.0g 该硝酸铵样品于容器中,滴入5.0g 20%的NaOH溶液.发生如下反应:NH4NO3+NaOH=NaNO3+NH3↑+H2O.反应过程中放出的氨气质量及加入的NaOH溶液的质量的关系如图所示:完成有关计算:
硝酸铵是农业生产中常用的化学肥料.为测定某含有少量NaNO3的硝酸铵样品中NH4NO3的纯度,取 2.0g 该硝酸铵样品于容器中,滴入5.0g 20%的NaOH溶液.发生如下反应:NH4NO3+NaOH=NaNO3+NH3↑+H2O.反应过程中放出的氨气质量及加入的NaOH溶液的质量的关系如图所示:完成有关计算:查看答案和解析>>
科目:初中化学 来源: 题型:
 实验室里,在一个具有刻度和可以滑动的活塞的玻璃管中放入白磷(过量,白磷燃烧所需的最低温度为40℃),将玻璃管固定好,放在盛有80℃热水的烧杯上,实验装置如图所示,试回答下列问题.
实验室里,在一个具有刻度和可以滑动的活塞的玻璃管中放入白磷(过量,白磷燃烧所需的最低温度为40℃),将玻璃管固定好,放在盛有80℃热水的烧杯上,实验装置如图所示,试回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com