��ѧ��ȤС���ͬѧ��ʵ��������ͼ��ʾ��װ���Ʊ����ֳ��������壮

��1��д��ͼ�б��Тٺ͢۵��������ƣ���
�Թ�
�Թ�
����
��ƿ
��ƿ
��2��С��ͬѧ�ø��������ȡ��������ѡ����Aװ�ã���ʹ����һС����������Ϊ�ռ��������ѡ��װ��
E
E
���÷�Ӧ�Ļ�ѧ����ʽ��
��
��3��С��ͬѧ�ù�������Ͷ������̻����ȡ����������Ϊ��Ӧ��ѡ���װ����
B
B
��ʵ����ѡ�ö������̵�������
������
������
���÷�Ӧ�Ļ�ѧ����ʽ��
ʵ�������С��˵�����ô����ǵ�ľ�����뼯��ƿ�ڣ�Ϊʲô���Ḵȼ�����������С���Ʋ�����������ԭ��
װ��©��
װ��©��
��дһ��ԭ�ɣ���
��4��С��ͬѧҲ��ȡ��һ�����壬��ֻ����Dװ���ռ�������Ϊ������Ӧ����
CO2
CO2
���������ʻ�ѧʽ�����÷�Ӧ�Ļ�ѧ����ʽ��
CaCO3+2HCl�TCaCl2+H2O+CO2��
CaCO3+2HCl�TCaCl2+H2O+CO2��
��5��С��ͬѧҲ��ȡ��һ�����壬�üȿ�����Eװ���ռ���Ҳ����Fװ���ռ�������Ϊ�����������
H2
H2
���������ʻ�ѧʽ��





 20��ijУ��ѧ��ȤС���ͬѧ���Ķ�����ʱ���֣�18����ĩ��������ѧ��������������������-��ʵ�飺��ˮ����ͨ��һ���պ��ǹ�ܣ�������һ�����壮ͬѧ�Ƕ����ʵ��ܸ���Ȥ���ѵ����ȵ�������ˮ������Ӧ�����ɵ���������ʲô��������Щ���ʣ��������������ͼ��ʾ��װ�ý���̽����
20��ijУ��ѧ��ȤС���ͬѧ���Ķ�����ʱ���֣�18����ĩ��������ѧ��������������������-��ʵ�飺��ˮ����ͨ��һ���պ��ǹ�ܣ�������һ�����壮ͬѧ�Ƕ����ʵ��ܸ���Ȥ���ѵ����ȵ�������ˮ������Ӧ�����ɵ���������ʲô��������Щ���ʣ��������������ͼ��ʾ��װ�ý���̽����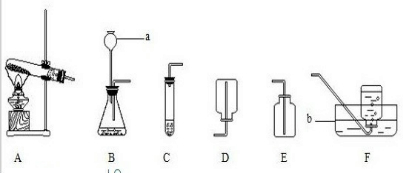
 ��2012?̫ԭ��ij��ѧ��ȤС���ͬѧ��̽��Mg��Cu��Fe���ֽ������й�����ʱ����������ʵ�飺
��2012?̫ԭ��ij��ѧ��ȤС���ͬѧ��̽��Mg��Cu��Fe���ֽ������й�����ʱ����������ʵ�飺