
| 元素名称 | ______ | 镁 | 银 | ______ | 锰 | ______ |
| 元素符号 | K | ______ | ______ | Hg | ______ | Cl |
| 物质名称 | 氧气 | ______ | 氢气 | ______ | 二氧化锰 | ______ |
| 化学式 | ______ | SO2 | ______ | P2O5 | ______ | Ba(OH)2 |
| 元素名称 | 钾 | 镁 | 银 | 锰 | 氯 | |
| 元素符号 | K | Mg | Ag | Hg | Mn | Cl |
| 物质名称 | 氧气 | 二氧化硫 | 氢气 | 五氧化二磷 | 二氧化锰 | 氢氧化钡 |
| 化学式 | O2 | SO2 | H2 | P2O5 | Mn | Ba(OH)2 |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
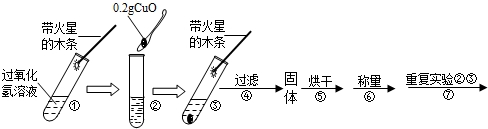
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
带火星的木条复燃. |
溶液中有气泡放出, |
猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立. |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 组别 | A组 | B组 | C组 |
| 分类标准 | 纯净物 | 碱 | 盐 盐 |
| 不属上述分类标准的物质 | 空气 | H2SO4 H2SO4 |
SO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
| KCl | CaCl2 | NaCl | MgCl2 | A1C13 | ZnCl2 ZnCl2 |
FeCl2 FeCl2 |
CuCl2 CuCl2 |


查看答案和解析>>
科目:初中化学 来源: 题型:
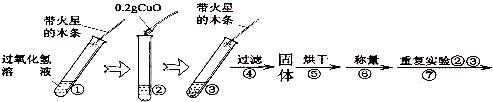
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中 有气泡放出 有气泡放出 带火星的木条复燃. |
0.2g 0.2g |
溶液中有气泡放出, 带火星的木条复燃 带火星的木条复燃 |
猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立. |
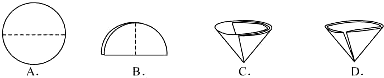
查看答案和解析>>
科目:初中化学 来源: 题型:
| A组 | B组 | C组 | D组 | E组 | |
| 分类标准 | 金属氧化物 | ② |
金属单质 | ④ |
⑤ |
| 不属于该类别的物质 | ① |
Cu | ③ |
H2O | ⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com