
(7分)将0.5g二氧化锰与一定量氯酸钾共热到质量不减少为止,称得残渣质量为15.4g。求:(1)生成氧气多少克? (2)原氯酸钾的质量是多少克?
(1)9.6克 (2)24.5克
【解析】
试题分析:根据质量守恒定律进行分析.根据氯酸钾分解的化学方程式可知,残渣是氯化钾和二氧化锰的混合物,由二氧化锰的质量可以计算出生成氯化钾的质量,由氯化钾的质量再根据上述反应就可以计算出生成氧气的质量.
解:由题意可知,残渣是氯化钾和二氧化锰的混合物,则氯化钾的质量为15.4g-0.5g=14.9g
设氧气的质量为x,原氯酸钾的质量为y,
2KClO3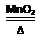 2KCl+3
O2
2KCl+3
O2 ↑
↑
245 149 96
y 14.9g x
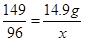
解得:x=9.6g
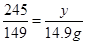
解得y=24.5g
答:生成9.6g氧气,原有氯酸钾24.5克。
考点:质量守恒定律及其应用。
点评:本题主要考查有关化学方程式的计算,解题时要注意残渣中含有催化剂二氧化锰.


科目:初中化学 来源: 题型:
| ||
| △ |
查看答案和解析>>
科目:初中化学 来源:《第5章化学方程式》2012年单元测试卷(高州中学)(解析版) 题型:解答题
查看答案和解析>>
科目:初中化学 来源:《第5单元 化学方程式》2010年单元测试卷(8)(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com