
分析 (1)根据锌和盐酸反应生成氯化锌和氢气进行分析;
(2)根据质量守恒定律计算生成氢气的质量;
(3)根据氢气的质量和化学方程式计算参加反应的锌的质量;
(4)根据计算出的锌的质量计算铜的质量分数;
(5)根据元素守恒进行计算.
解答 解:(1)锌和盐酸反应生成氯化锌和氢气,化学方程式为:Zn+2HCl═ZnCl2+H2↑;
(2)生成氢气的质量为:100g+100g-199.2g=0.8g;
(3)设黄铜样品中锌的质量为x
Zn+2HCl═ZnCl2+H2↑
65 2
x 0.8g
$\frac{65}{x}$=$\frac{2}{0.8g}$
x=26g
(4)黄铜样品中铜的质量分数是:$\frac{100g-26g}{100g}$×100%=74%;
(5)设可炼得这种黄铜的质量为y
Cu2O-------2Cu
144 128
288t×60% y×74%
$\frac{144}{288t×60%}$=$\frac{128}{y×74%}$
y=208t
故答案为:(1)Zn+2HCl═ZnCl2+H2↑;
(2)0.8g;
(3)$\frac{65}{x}$=$\frac{2}{0.8g}$;
(4)黄铜样品中铜的质量分数是74%;
(5)可炼得这种黄铜的质量为208t.
点评 本题考查根据化学方程式的简单计算,已知生成物的质量求反应物的质量.


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
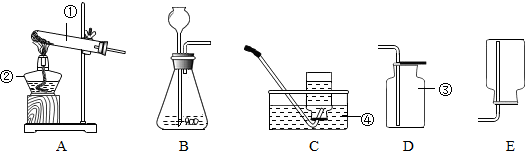
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 打火机给人们的生活带来了方便,电子打火机的构造如图所示,请回答以下问题:
打火机给人们的生活带来了方便,电子打火机的构造如图所示,请回答以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | $\frac{12n}{m}$ | B. | $\frac{12m}{n}$ | C. | $\frac{n}{12m}$ | D. | $\frac{m}{12n}$ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
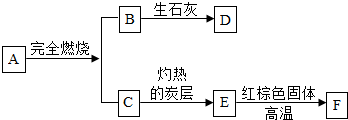
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com