
分析 纯净物是指由一种物质组成的物质;活性炭具有吸附性;肥皂水用来检验硬水和软水;常用的净化水的方法有沉淀、过滤、吸附、蒸馏等.
解答 解:(1)矿泉水、自来水和河水含有水和其他的杂质,由多种物质组成,属于混合物,蒸馏水只有一种物质水组成,属于纯净物.
故填:蒸馏水;
(2)活性炭具有吸附性,能吸附色素和异味.活性炭在净化水的过程中主要利用了它的吸附性.
故填:吸附;
(3)肥皂水用来检验硬水和软水.
故填:肥皂水;
(4)常用的净化水的方法有沉淀、过滤、吸附、蒸馏等.其中沉淀、过滤、吸附只能除去水中部分杂质,蒸馏得到的水是纯水,是净化程度最高的方法.
故填:沉淀、过滤、吸附、蒸馏等.
点评 本题考查了常见的净水的知识,完成此题,可以依据物质的性质进行.


科目:初中化学 来源: 题型:计算题
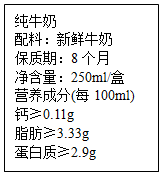 人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体[Ca10(PO4)6(OH)2]形式存在,其相对分子质量为1004.牛奶含钙丰富又易吸收,且牛奶中钙和磷比例合适,是健骨的理想食品.如图是某乳业公司纯牛奶包装标签的部分文字.请仔细阅读后回答下列问题.
人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体[Ca10(PO4)6(OH)2]形式存在,其相对分子质量为1004.牛奶含钙丰富又易吸收,且牛奶中钙和磷比例合适,是健骨的理想食品.如图是某乳业公司纯牛奶包装标签的部分文字.请仔细阅读后回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
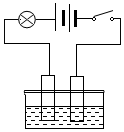 如图所示,烧杯中装有蒸馏水,
如图所示,烧杯中装有蒸馏水,查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
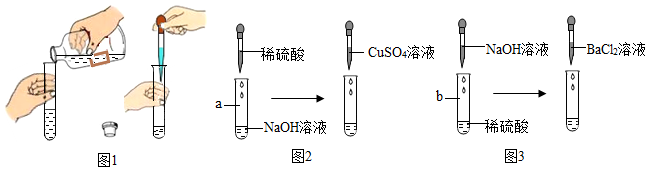
| 实验步骤 | 实验现象 | 实验结论 |
| 在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量反应后的溶液滴在pH试纸上,把试纸显示的颜色与标准比色卡比较,读溶液的pH | pH<7 (填“>”、“=”或“<”) | 稀硫酸与氢氧化钠溶液发生了反应,且稀硫酸过量了. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO和C60都属于化合物 | B. | 氮气和氧气都属于非金属单质 | ||
| C. | H2O和C2H5OH都属于氧化物 | D. | 自来水和蒸馏水都属于纯净物 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
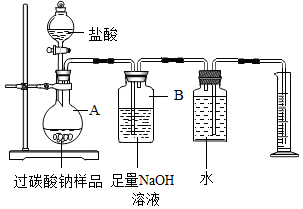 “氧泡泡”系列产品去污能力强、绿色环保,已成为中国氧系清洁品类领导品牌,其主要成分是过碳酸钠(2Na2CO3•3H2O2).某化学活动小组对过碳酸钠产生了浓厚的兴趣,决定对其进行探究.
“氧泡泡”系列产品去污能力强、绿色环保,已成为中国氧系清洁品类领导品牌,其主要成分是过碳酸钠(2Na2CO3•3H2O2).某化学活动小组对过碳酸钠产生了浓厚的兴趣,决定对其进行探究.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com