
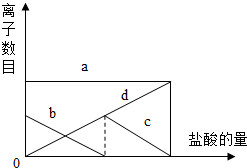
 向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌,发现开始没产生气泡,盐酸加到一定程度才产生气泡.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是( )
向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌,发现开始没产生气泡,盐酸加到一定程度才产生气泡.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是( )| A. | a:Cl-; b:K+; c:CO${\;}_{3}^{2-}$; d:HCO${\;}_{3}^{-}$ | |
| B. | a:K+; b:CO${\;}_{3}^{2-}$; c:Cl-; d:HCO${\;}_{3}^{-}$ | |
| C. | a:K+; b:CO${\;}_{3}^{2-}$; c:HCO${\;}_{3}^{-}$; d:Cl- | |
| D. | a:K+; b:HCO${\;}_{3}^{-}$; c:Cl-; d:CO${\;}_{3}^{2-}$ |
分析 因考虑K2CO3在溶液中电离出K+和CO32-,盐酸溶液中存在H+、Cl-,因而出现CO32-+ H+═HCO3-,然后HCO3-+ H+═H2O+CO2,因向一定量的K2CO3溶液中缓慢地滴加稀盐酸,即出现如图现象.
解答 解:A、因在碳酸钾溶液中K2CO3═2K++CO32-,所以溶液开始就存在K+和CO32并且K+和CO32-的个数比为2:1,根据图象显示,CO32-+ H+═HCO3-因而CO32-不断减少,因而a 为 K+,b 为 CO32-. 故A不正确.
B、当向一定量的K2CO3溶液中缓慢地滴加稀盐酸,溶液中出现H+、Cl-,并且CO32-+ H+═HCO3-,H++HCO3-═H2CO3.碳酸分解生成水和二氧化碳,这就是向一定量的K2CO3溶液中缓慢地滴加稀盐酸,不断搅拌,发现开始没产生气泡的原因;结合 A 项选答,故B 不正确.
C、盐酸加到一定程度才产生气泡是因为碳酸开始分解的缘故,生成的KCl在溶液中仍存在Cl-;因而Cl-在图象中随着加盐酸就出现了,所以d必代表Cl-.随着碳酸的不断分解,HCO3-逐渐减少直到消失.因而c必代表HCO3-.故C 正确.
D、通过以上选项分析解答,故D 不正确.
故选 C.
点评 此题既考查学生对酸的性质理解运用,有渗透离子反应的实质,还锻炼学生的良好推断能力.可谓难题.


 智能训练练测考系列答案
智能训练练测考系列答案科目:初中化学 来源: 题型:选择题
| A. | 可用纯碱与石灰水制烧碱 | B. | 它们易溶于水 | ||
| C. | 它们都是烹调调味品 | D. | 它们加酸都能放出二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验方案 | 使用的试剂 | 判断的方法 |
| A | 铁粉 | 如果有气泡产生,表明盐酸已经过量 |
| B | pH试纸 | 如果pH<7,表明盐酸已经过量 |
| C | 无色酚酞试剂 | 如果溶液变成不变色,表明盐酸已经过量 |
| D | 紫色石蕊试剂 | 如果溶液变成红色,表明盐酸已经过量 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
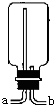 实验室开放日,我与小娜、小佳、小华、小丽等同学来到实验室,看到实验桌上摆放着四瓶无标签的试剂,分别是两瓶固体和两瓶液体,我们决定对“固体与液体”之间的反应进行一些探究.
实验室开放日,我与小娜、小佳、小华、小丽等同学来到实验室,看到实验桌上摆放着四瓶无标签的试剂,分别是两瓶固体和两瓶液体,我们决定对“固体与液体”之间的反应进行一些探究.| 实验步骤 | 实验现象 | 实验结论 |
| 将气体通入澄清石灰水中 | 澄清的石灰水变浑浊 | 证明该气体是二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
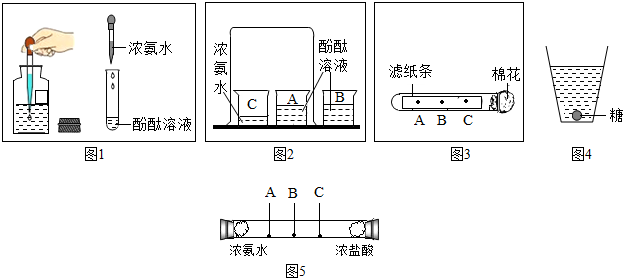
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
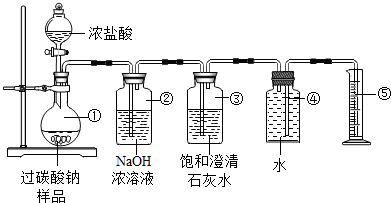
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ②③ | D. | ①③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com