
分析 大理石的主要成分为碳酸钙,与盐酸反应生成氯化钙、水和二氧化碳,根据反应的化学方程式,由参加反应的盐酸的质量可计算生成二氧化碳的质量;利用质量与体积的关系:m=ρV,由二氧化碳的质量计算出二氧化碳的体积.
解答 解:设生成二氧化碳的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 44
50g×14.6% x
$\frac{73}{50g×14.6%}=\frac{44}{x}$
x=4.4g
标准状况下二氧化碳的体积为:$\frac{4.4g}{1.977g/L}$≈2.2L
答:生成二氧化碳的质量是4.4g,这些二氧化碳的体积(标准状况)是2.2L.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.


科目:初中化学 来源: 题型:选择题
| A. | NO3- H+ Na+ OH- | B. | K+ SO42- Na+ NO3- | ||
| C. | Cl- K+ SO42- Ba2+ | D. | Ca2+ Cl- CO32- K+ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入紫色石蕊试液 | 试液不变红 | 恰好中和 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 由两种物质生成一种物质的反应叫做化合反应 | |
| B. | 工业制氧气的方法是分离液态空气,为分解反应 | |
| C. | 石蜡的燃烧属于氧化反应,但不属于化合反应 | |
| D. | 在空气中不能燃烧的物质,在氧气中也不能燃烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
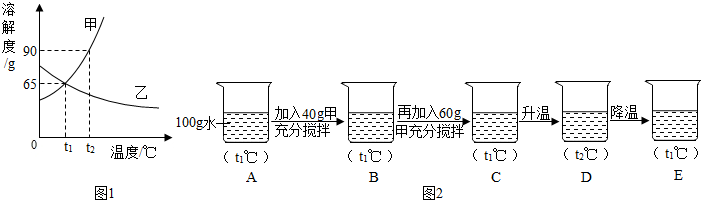
 如图是甲、乙两种固体的溶解度曲线,回答问题:
如图是甲、乙两种固体的溶解度曲线,回答问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com