
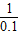 =
=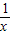


 53随堂测系列答案
53随堂测系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 序号 | 守恒 | 相应的解释 |
| 1 | 例如:溶质守恒 | 溶质的质量在溶液稀释前后不发生改变 |
| 2 | 质量守恒 | 参加化学反应的各物质的质量总和等于生成的各物质的质量总和 参加化学反应的各物质的质量总和等于生成的各物质的质量总和 |
| 3 | 元素守恒 元素守恒 |
化学反应前后元素的种类(质量)不变 化学反应前后元素的种类(质量)不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 步骤 | 实验操作 | 实验结果 |
| 1 | 取100mL水,加入20g硝酸钾,搅拌,恢复至20℃ | 全部溶解,得溶液① |
| 2 | 再加11.6g硝酸钾,搅拌,恢复至20℃ | 恰好饱和,得溶液② |
| 3 | 再加20g硝酸钾,搅拌,恢复至20℃ | 得溶液③ |
| 4 | 加热 | 全部溶解,得溶液④ |
| 5 | 冷却至20℃ | 析出晶体,得溶液⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| △ |
| ||
| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com