课外化学兴趣小组的同学利用某化工厂的废碱液(主要成分为Na
2CO
3,还含有少量NaCl,其它杂质不计)和石灰乳为原料制备烧碱,并对所得的烧碱粗产品的成分进行分析和测定.
【粗产品制备】
(1)将废碱液加热蒸发浓缩,形成较浓的溶液,冷却后与石灰乳混合,发生反应的化学方程式为
Na2CO3+Ca(OH)2═2NaOH+CaCO3↓
Na2CO3+Ca(OH)2═2NaOH+CaCO3↓
.
(2)将反应后的混合物过滤,得到的滤液进行蒸发结晶,制得NaOH粗产品.
【粗产品成分分析】
(1)取适量粗产品溶于水,滴加Ba(NO
3)
2溶液出现白色浑浊,发生反应的化学方程式为
Ba(NO3)2+Na2CO3═BaCO3↓+2NaNO3
Ba(NO3)2+Na2CO3═BaCO3↓+2NaNO3
,该粗产品中一定不含有
氢氧化钙
氢氧化钙
,理由是
滴加硝酸钡产生沉淀,说明产品中含有碳酸钠,碳酸钠能与氢氧化钙发生反应,二者不能共存
滴加硝酸钡产生沉淀,说明产品中含有碳酸钠,碳酸钠能与氢氧化钙发生反应,二者不能共存
.
(2)该小组同学通过对粗产品成分的实验分析,确定该粗产品中含有三种物质.
【粗产品中Na
2CO
3含量测定】
(1)该兴趣小组的同学设计了下图所示的实验装置.取10.0g粗产品,进行实验.

(2)操作步骤
①连接好装置,检查气密性;②打开弹簧夹C,在A处缓缓通入一段时间空气;③称量G的质量;④关闭弹簧夹C,慢慢滴加浓盐酸至过量,直至D中无气泡冒出;⑤打开弹簧夹 C,再次缓缓通入一段时间空气;⑥再次称量G的质量,得前后两次质量差为0.48g.
(3)问题探究
①步骤②的目的是
排除装置内的空气,防止含有的二氧化碳对实验结果造成干扰
排除装置内的空气,防止含有的二氧化碳对实验结果造成干扰
;
②B装置的作用是
吸收空气中的二氧化碳
吸收空气中的二氧化碳
,F中的试剂应为
浓硫酸
浓硫酸
;
③E 装置的作用是
吸收除去挥发出的氯化氢气体
吸收除去挥发出的氯化氢气体
,相关反应的化学方程式是
NaHCO3+HCl═NaCl+H2O+CO2↑
NaHCO3+HCl═NaCl+H2O+CO2↑
,H装置的作用是
吸收空气中的二氧化碳
吸收空气中的二氧化碳
.若没有H装置,则测定的Na
2CO
3的质量分数会
偏大
偏大
(填“偏大”、“偏小”、“不变”).事实上10.0g粗产品只能产生0.44g CO
2.请你仔细分析上述实验,解释实验值0.48g比正确值0.44g偏大的原因(假设操作均正确)
装置D中浓盐酸挥发出的氯化氢与装置E中NaHCO3反应产生二氧化碳
装置D中浓盐酸挥发出的氯化氢与装置E中NaHCO3反应产生二氧化碳
.




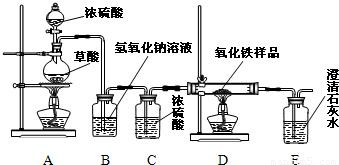
 某校化学课外兴趣小组的同学在研究性学习课上展示了一套如下图所示实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:H2C2O4
某校化学课外兴趣小组的同学在研究性学习课上展示了一套如下图所示实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:H2C2O4

 某校化学课外兴趣小组的同学在研究性学习课展示了一套如图所示的实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:
某校化学课外兴趣小组的同学在研究性学习课展示了一套如图所示的实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应: CO↑+CO2↑+H2O
CO↑+CO2↑+H2O