
ij»ÆѧѧĻ°ŠĖȤŠ”×éĪŖĮĖ²ā¶ØÄ³ÉśĄķŃĪĖ®µÄČÜÖŹÖŹĮæ·ÖŹż£¬ŹµŃé¹ż³ĢŗĶÓŠ¹ŲŹµŃ鏿¾ŻČēĶ¼ĖłŹ¾£ŗ

øł¾ŻÉĻĶ¼ŠÅĻ¢½ā¾öĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŅŃÖŖ¹żĀĖŗó»ńµĆµÄ¹ĢĢåĪļÖŹŹĒŅ»ÖÖ“æ¾»Īļ£¬ŌņøĆĪļÖŹµÄĆū³ĘŹĒ____________£¬ÖŹĮæŹĒ__________g”£
£Ø2£©øĆÉśĄķŃĪĖ®µÄČÜÖŹÖŹĮæ·ÖŹżŹĒ¶ąÉŁ£æ£ØŠ“³öŌĖĖć¹ż³Ģ£©________________
£Ø3£©ĒėŌŚĶ¼ÉĻ×÷³öĶłÉśĄķŃĪĖ®µĪ¼Ó AgNO3 ČÜŅŗ£¬ ²śÉś AgCl ³ĮµķµÄÖŹĮæÓė²ĪÓė·“Ó¦µÄ AgNO3 ČÜŅŗµÄÖŹĮæÖ®¼äµÄ¹ŲĻµĶ¼Ļń”£__________
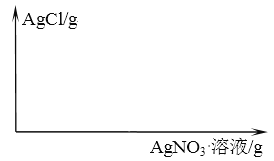
£Ø4£©ŅŃÖŖĻõĖįÄʵÄČܽā¶ČČē±ķĖłŹ¾£¬¾Ż“Ė¹ĄĖćÅŠ¶ĻøĆŹµŃé»ńµĆµÄ 161.13g ČÜŅŗŌŚ³£ĪĀĻĀŹōÓŚ___________________ČÜŅŗ£ØĢī”°±„ŗĶ”±»ņ”°²»±„ŗĶ”±£©”£
ĻõĖįÄĘŌŚĖ®ÖŠµÄČܽā¶Č
ĪĀ¶Č/”ę | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
Čܽā¶Č/g | 73 | 80 | 87 | 98 | 103 | 113 | 124 | 137 | 150 | 163 | 180 |
 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ¹ć¶«Ź”2019½ģ¾ÅÄź¼¶ĻĀѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
Å·ĆĖ¹ś¼ŅŅŃ½ūÓĆĖ®ŅųĪĀ¶Č¼Ę£¬ŅņĪŖĖüŌŚŹ¹ÓĆŹ±Ņ×ĘĘĖé¶ųŠ¹Ā©Ė®ŅųĪ£ŗ¦ČĖĢ彔浔£Ė®ŅųŹōÓŚ£Ø £©
A. »ÆŗĻĪļ B. Ńõ»ÆĪļ C. µ„ÖŹ D. »ģŗĻĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ½ĖÕŹ”ÄĻĶØŹŠ2019½ģ¾ÅÄź¼¶ĻĀѧʌ3ŌĀ½×¶ĪŠŌĮ·Ļ°»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĮ÷³ĢĢā
ĻÖ“śŃ»·¾¼ĆŅŖĒó×ŪŗĻæ¼ĀĒ»·¾³ĪŪČ¾ŗĶ¾¼ĆŠ§Ņę”£øß“æŃõ»ÆĢśæÉ×÷ĻÖ“śµē×Ó¹¤ŅµµÄ²ÄĮĻ,ŅŌĻĀŹĒÓĆĮņĢśæóÉÕŌü(Ö÷ŅŖ³É·ÖĪŖFe2O3”¢FeO”¢SiO2)ĪŖŌĮĻÖʱøøß“æŃõ»ÆĢś(Fe2O3)µÄÉś²śĮ÷³ĢŹ¾ŅāĶ¼£¬[(NH4)2CO3]ČÜŅŗ³Ź¼īŠŌ,40”ęŅŌÉĻŹ±[(NH4)2CO3]·Ö½ā)£ŗ

(1)ŹµŃéŹŅÖŠ,²Ł×÷¢ń”¢²Ł×÷¢ņÓƵ½µÄ²£Į§ŅĒĘ÷ÓŠ²£Į§°ō”¢ÉÕ±”¢_______µČ.
(2)ĀĖŅŗ¢ńÖŠÖ÷ŅŖµÄŃōĄė×ÓŹĒ_______µČ.
(3)¼ÓŹŹĮæ°±Ė®µÄÄæµÄŹĒ_____________________.
(4)øł¾ŻĢāÖŠŠÅĻ¢,¼ÓČė[(NH4)2CO3]ŗó,øĆ·“Ó¦±ŲŠėæŲÖʵÄĢõ¼žŹĒ______________.
(5)ĀĖŅŗ¢ņÖŠæÉ»ŲŹÕµÄ²śĘ·ŹĒ_________(Š“»ÆѧŹ½),øĆĪļÖŹµÄÓĆĶ¾ŹĒ___________.
(6)Š“³öŌŚæÕĘųÖŠģŃÉÕFeCO3µÄ»Æѧ·“Ó¦·½³ĢŹ½_________________.
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ½ĖÕŹ”ĖŽĒØŹŠ2019½ģ¾ÅÄź¼¶ĻĀѧʌ£ØµŚĘß“Ī£©Ń§Ēéµ÷ŃŠ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
Éś»īÖŠ“¦“¦ÓŠ»Æѧ£¬»ÆѧÓėÉś»ī”¢Éś²śĆÜĒŠĻą¹Ų”£
£Ø1£©ŗ£Ģ¦°ü×°“üÖŠ³£ÓƵÄøÉŌļ¼ĮĪŖŅ»ÖÖŃõ»ÆĪļ£¬Š“³öøĆĪļÖŹµÄ»ÆѧŹ½_____£»
£Ø2£©ĪøĄļŗ¬ÓŠµÄÄÜ°ļÖśĻū»ÆµÄĖįĪŖ_____£ØĢīĆū³Ę£©£»
£Ø3£©×ŌČ»½ēµÄĖ®¶¼ĪŖ»ģŗĻĪļ£¬Éś»īÖŠ³£ÓĆ_____·Ø½«Ó²Ė®×Ŗ»ÆĪŖČķĖ®”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ½ĖÕŹ”ĖŽĒØŹŠ2019½ģ¾ÅÄź¼¶ĻĀѧʌ£ØµŚĘß“Ī£©Ń§Ēéµ÷ŃŠ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
×ī½ü£¬ĪŅ¹śæĘѧ¼Ņ³É¹¦ŗĻ³ÉŠĀŠĶ“߻ƼĮ£¬½«CO2øߊ§×Ŗ»ÆĪŖ¼×“¼£ØCH3OH£©£¬øĆ»Æѧ·“Ó¦µÄĪ¢¹Ū¹ż³ĢČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©

A. ¼×”¢±ūĮ½ÖÖĪļÖŹ¾łĪŖÓŠ»śĪļ B. ·“Ó¦Ē°ŗóHŌŖĖŲ»ÆŗĻ¼Ū²»±ä
C. ²Ī¼Ó·“Ó¦µÄ¼×”¢ŅŅĮ½ĪļÖŹÖŹĮæ±ČĪŖ22”Ć3 D. ·“Ó¦Ē°ŗóŌ×ÓŹżÄæ·¢Éśøıä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ¹ć¶«Ź”½ŅŃōŹŠæÕøŪĒų2019½ģ¾ÅÄź¼¶ĻĀѧʌŅ»Ä£æ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
¹éÄÉŹĒѧĻ°µÄÖŲŅŖ·½·Ø”£Ń§ĶźŃĪµÄŠŌÖŹŗ󣬊”Ö£¹éÄɳöĖįµÄ A”¢B”¢C”¢D”¢E ĪåĢõ»ÆѧŠŌÖŹ£¬²¢ÓĆ”°Īå½ĒŠĒ”±³ŹĻÖ³öĄ“£¬¼ūĻĀĶ¼£ŗ
£Ø1£©Ķ¼ÖŠĖįµÄ D ŠŌÖŹÖŠ£¬¼“”°Īå½ĒŠĒ”±ÓŅĻĀ½ĒĄļĆę¶ŌÓ¦ĪļÖŹµÄĄą±šŹĒ____________£»

£Ø2£©×ĻÉ«ŹÆČļŹŌŅŗµĪČėĖįÖŠ£¬ČÜŅŗĻŌ_____________É«£»
£Ø3£©ČōĖįŹĒĮņĖį£¬ĒėŠ“³öÓĆĻ”ĮņĖįĒå³żĢśŠāµÄÖ÷ŅŖ·“ Ó¦»Æѧ·½³ĢŹ½£ŗ________________£»
£Ø4£©ČōĖįŹĒŃĪĖį£¬ĒėÄćŃ”ŌńŅ»ÖÖ³£¼ūµÄĪļÖŹĄ“¼ģŃéĖį µÄ D ŠŌÖŹ___________________£ØĢī»ÆѧŹ½£©£»
£Ø5£©Š”Ö£Ģ½¾æ Mg ŗĶ Fe ÓėĖįŅŗ·“Ó¦µÄæģĀż£¬ŠčŅŖæŲÖʵıäĮæŹĒ______________________(Ģī“śŗÅ)”£
¢Ł½šŹōµÄ¾Ū¼ÆŠĪĢ¬£ØŠĪד£©£»¢ŚĖįŅŗĘšŹ¼ĪĀ¶Č£»¢ŪĖįŅŗÖÖĄą£»¢ÜĖįŅŗµÄÅØ¶Č£»¢Ż·“ӦȯĘ÷µÄ“óŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ¹ć¶«Ź”½ŅŃōŹŠæÕøŪĒų2019½ģ¾ÅÄź¼¶ĻĀѧʌŅ»Ä£æ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
¹éÄÉ·ØŹĒѧĻ°»ÆѧµÄÖŲŅŖ·½·ØÖ®Ņ»£¬ĻĀĮŠĶ¼Ź¾ÕżČ·µÄŹĒ
|
|
|
|
A£®»Æѧ·“Ó¦·ÖĄą | B£® ĪļÖŹ·ÖĄą | C£®µŲæĒÖŠŌŖĖŲŗ¬Įæ | D£®½šŹōµÄ»ÆѧŠŌÖŹ |
A. A B. B C. C D. D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ¹ć¶«Ź”Ć·ÖŻŹŠ2019½ģ¾ÅÄź¼¶ĻĀѧʌµŚ¶žŃ§ĘŚµŚ¶ž“ĪÖŹ¼ģ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĮ÷³ĢĢā
·ĻĢśŠ¼µÄÖ÷ŅŖ³É·ÖŹĒĢś£¬Ķ¬Ź±»¹ÓŠÉŁĮæĢśŠā£ØÖ÷ŅŖ³É·ÖŹĒFe2O3£©µČŌÓÖŹ£¬¶ÆĪļĖĒĮĻĮņĖįŃĒĢśµÄÉś²ś¹¤ŅÕÖ®Ņ»ČēĶ¼ĖłŹ¾£ŗ
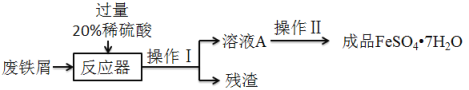
£Ø1£©ŹµŃéŹŅÓūÓĆ98%µÄÅØĮņĖį£ØĆܶČ1.84g/mL£©ÅäÖĘ200g20%µÄĻ”ĮņĖį£¬ÓŠŅŌĻĀŹµŃé²½Öč£ŗ
a.ĮæČ” b.¼ĘĖć c.Ļ”ŹĶ d.×°ĘæĢł±źĒ©
ÕżČ·µÄĖ³ŠņŹĒ_____£ØĢī×ÖÄø£©”£ČōÓĆĮæĶ²ĮæČ”ÅØĮņĖįŹ±ø©ŹÓ¶ĮŹż£¬ĘäĖū²Ł×÷ÕżČ·£¬ŌņĖłµĆČÜŅŗµÄÖŹĮæ·ÖŹż_____20%£ØĢī”°£¾”±”°£¼”±»ņ”°£½”±£©”£
£Ø2£©ŌŚ·“Ó¦Ę÷ÖŠ·“ÉśµÄ»Æѧ·“Ó¦¢ŁFe2O3£«3H2SO4£½Fe2(SO4)3£«3H2O£»¢ŚFe2(SO4)3£«Fe£½3FeSO4£»¢Ū_____”£
£Ø3£©ČÜŅŗAÖŠµÄČÜÖŹŹĒ_____£ØĢī»ÆѧŹ½£©”£
£Ø4£©²Ł×÷¢ńµÄĆū³ĘŹĒ_____£¬Ķź³É²Ł×÷¢ńµÄ²£Į§ŅĒĘ÷ÓŠ£ŗ²£Į§°ō”¢ÉÕ±ŗĶ_____”£
£Ø5£©¾¹ż²Ł×÷¢ņ£ŗÕō·¢ÅØĖõ”¢_____”¢¹żĀĖ”¢±łĖ®Ļ“µÓ”¢µĶĪĀøÉŌļæɵĆĮņĖįŃĒĢś¾§Ģå£ØFeSO4•7H2O£©£¬ÓƵĶĪĀøÉŌļĖµĆ÷ĮņĖįŃĒĢś¾§ĢåæÉÄܾßÓŠµÄŠŌÖŹŹĒ_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ¹ć¶«Ź”2019½ģ¾ÅÄź¼¶ĻĀŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
2016Äź2ŌĀ16ČÕ”¶æĘ¼¼Čձؔ·±ØµĄ£¬ĆĄ¹śÓĢĖū“óѧ¹¤³ĢŹ¦·¢ĻÖĮĖŠĀŠĶ¶žĪ¬°ėµ¼Ģå²ÄĮĻŅ»Ńõ»ÆĪż£ØSnO£©£¬ÓŠĶū½«µē×ÓÉč±øĖŁ¶ČĢįøß100±¶£¬ŌņŅ»Ńõ»ÆĪżÖŠĪżŌŖĖŲµÄ»ÆŗĻ¼ŪŹĒ£Ø £©
A. ©2 B. ©1 C. +1 D. +2
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com