

分析 (1)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.因此完全反应后,物质减少的质量就是生成的气体质量;
(2)根据过氧化氢分解的化学方程式和(1)中计算出的氧气的质量,就可计算出参与反应的过氧化氢的质量,然后根据质量分数公式计算即可.
(3)根据反应后剩余混合物中氢元素存在于水中分析;
解答 解:(1)二氧化锰不溶于水,根据质量守恒定律,反应生成氧气的质量=50.0g+1.0g-49.4g=1.6g.
(2)解:设过氧化氢溶液中含有过氧化氢的质量为x.
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 1.6g
$\frac{68}{x}=\frac{32}{1.6g}$
解之得:x=3.4g,
过氧化氢的质量分数为:$\frac{3.4g}{50.0g}$×100%=6.8%,
(3)反应后剩余混合物中氢元素存在于水中.氢元素的质量为:(49.4g-1.0g)×$\frac{2}{18}×100%$=5.4g
答案:
(1)1.6g;
(2)该过氧化氢溶液中溶质的质量分数为6.8%.
(3)5.4g.
点评 本题主要考查学生根据质量守恒定律,运用化学方程式和质量分数公式进行计算的能力.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
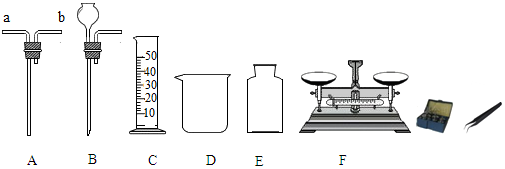
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 澄清的矿泉水是纯水 | B. | 肥皂水可鉴别硬水和软水 | ||
| C. | 过滤可以除去水中所有的杂质 | D. | 填埋垃圾不会导致水体污染 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红色铜丝表面变黑,是因为生成了氧化铜 | |
| B. | 红色铜丝表面变黑,是因为铜发生了还原反应 | |
| C. | 立即把变黑的铜丝插入稀硫酸中,溶液会出现蓝色 | |
| D. | 红色铜丝变为黑色后,总的质量增加 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
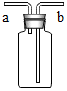 如图有多种功能,如收集气体、洗涤气体、贮存气体等.回答下列问题:
如图有多种功能,如收集气体、洗涤气体、贮存气体等.回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com