
【题目】化学研究小组在开展了“过氧化氢制取氧气的反应中二氧化锰的作用”之后,又进行了“寻找新的催化剂”的探究实验。
(提出问题 1)寻找“氧化铁能否用于过氧化氢溶液分解的催化剂”的证据?如果能, 它的催化效果如何?
(实验设计 1)
实 验 | 现 象 |
Ⅰ.分别量取 5 毫升 5%的过氧化氢溶液于 A、B 两支试管中,向 A 中加入 a 克氧化铁粉末,并分别在 A、B 两支试管中伸入带火星的木条,观察现象。 | A 试管中产生气泡,带火星的木条复燃,B 试管中无明显现象 |
Ⅱ.将“实验Ⅰ”中 A 试管的剩余物质分离,将所得固体进行洗涤、干燥、称量 | 所得固体质量为 a 克 |
Ⅲ.将“实验Ⅱ”得到的固体放入盛有 5 毫升 5%的过氧化氢溶液的试管中,向试管中伸入带火星的木条 | 有气泡冒出,带火星的木条复燃 |
Ⅳ.分别量取 5 毫升 5%的过氧化氢溶液放入 C、D 两 支试管中,向 C 试管中加入 a 克氧化铁粉末,向 D 试管中加入 a 克二氧化锰粉末 |
(实验结论)
(1)A 中产生的气体是_____;
(2)氧化铁可以作过氧化氢分解的催化剂,寻找该结论的证据主要是设计了实验_____(选填Ⅰ、Ⅱ、Ⅲ或Ⅳ)展开的。
(实验评价)
(1)设计实验Ⅲ的目的是_____;
(2)可以用下列方法作出判断,从而达到实验Ⅳ的设计目的。a.定性判断:观察 C、D两支试管中产生气泡的快慢;b.定量判断:_____。
(资料信息)过氧化氢分解除了用二氧化锰还可用氧化铜等物质作为催化剂
(提出问题 2)氧化铜(黑色粉末)是否也能作氯酸钾分解的催化剂?它是否比二氧化锰效果更好?
(实验设计 2)某同学以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
实验序号 | 氯酸钾质量 | 其他物质质量 | 待测数据 |
① | 1.2 克 | X | |
② | 1.2 克 | 氧化铜 0.5 克 | Y |
③ | m | 二氧化锰 0.5 克 | Z |
(1)写出氯酸钾在二氧化锰的催化作用下发生的反应的化学方程式:_____。
(2)上述实验应测量的“待测数据”是指_____,从数学描述角度,X、Y、Z 在数值上的大小关系是_____。
(3)若实验②比实验①的“待测数据”更_____(填“大”“小”或“不确定”),说明氧化铜能加快氯酸钾的分解速率。表中“m”的数值应该为_____。
(4)将实验②反应后的固体经过过滤、洗涤、干燥处理后,称量得到 0.5 克黑色粉末, 再将黑色粉末放入_____(简述操作)。
(总结提高)二氧化碳可用于灭火,但不是所有可燃物失火都可以用二氧化碳来扑灭。
【答案】氧气 Ⅰ、Ⅱ、Ⅲ 证明氧化铁的化学性质在化学反应前后保持不变 观察收集一试管气体所需时间的长短 2KClO3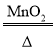 2KCl+3O2↑ 收集等量氧气所需时间 X>Y>Z 小 1.2 盛有适量的氯酸钾的试管中并加热,再用带火星的木条放在试管口,观察到木条迅速复燃
2KCl+3O2↑ 收集等量氧气所需时间 X>Y>Z 小 1.2 盛有适量的氯酸钾的试管中并加热,再用带火星的木条放在试管口,观察到木条迅速复燃
【解析】
[实验结论](1)A试管内的气体能使带火星的木条复燃,说明该气体是氧气;
(2)能够改变化学反应的速率,其质量与化学性质在反应前后保持不变的物质是该反应的催化剂,因此证明氧化铁可以作过氧化氢分解的催化剂,寻找该结论的证据主要是设计了实验Ⅰ、Ⅱ、Ⅲ展开的;
[实验评价](1)设计实验Ⅲ的目的是证明氧化铁的化学性质在化学反应前后保持不变;
(2))可以用下列方法作出判断,从而达到实验Ⅳ的设计目的。a、定性判断:观察C、D两支试管中产生气泡的快慢;b、定量判断:观察收集一试管气体所需时间的长短;
[设计实验2](1)氯酸钾在二氧化锰的催化作用下、加热分解为氯化钾和氧气;反应的化学方程式:2KClO3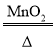 2KCl+3O2↑;
2KCl+3O2↑;
(2)本题的实验目的证明氧化铜能加快氯酸钾的分解,所以“待测数据”是收集等量氧气所需时间。实验①没有使用催化剂,所需时间最长,氧化铜的催化效果不如二氧化锰,所以实验③所需时间最短,即X>Y>Z;
(3)如果氧化铜能加快氯酸钾的分解速率,实验Ⅱ比实验I所用时间小。所取氯酸钾的质量应相同,即m=1.2g;
(4)实验②反应后溶解、过滤、洗涤、干燥后的黑色固体只有氧化铜,将黑色固体加入盛有适量的氯酸钾的试管中并加热,再用带火星的木条放在试管口,观察到木条迅速复燃。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】逻辑推理是一种重要的化学思维方法。下列推理合理的是( )
A. 因为碱溶液呈碱性,所以显碱性的溶液一定都是碱的溶液
B. 因为H2O和H2O2的组成元素相同,所以它们的化学性质相同
C. 置换反应中一定有单质生成,则有单质生成的化学反应一定是置换反应
D. 单质中只含有一种元素,但是只含有一种元素的物质不一定是单质
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业烟气脱硫就是将烟气中含有的二氧化硫除去,一种采用“双碱法”脱硫的工业流程示意图如下,下列说法错误的是
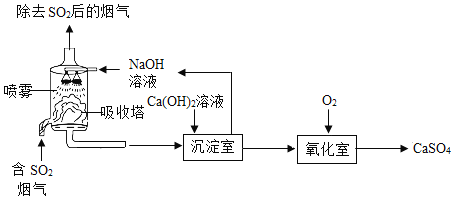
A.吸收塔中,NaOH溶液喷成雾状是为了增大接触面积能充分吸收SO2
B.氧化室中,化学反应的基本类型是氧化反应
C.沉淀室中,发生反应的化学方程式为Na2SO3+Ca(OH)2=CaSO3↓+2NaOH
D.上述流程中,可以循环利用的物质是NaOH和CaSO4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】武汉将成为我国首个新型氢能城市。某化学兴趣小组在老师的帮助下围绕氢气的燃烧实验开展如下探究:
(1)点燃氢气前,一定先要________。点燃纯净的氢气可以看到淡蓝色火焰现象,该反应的化学方程式为________,该反应的基本类型为______反应。
(2)研究氢气燃烧实验,需要用试管收集不同体积比的氢气与空气的混合物,若用试管(假设试管容积为10mL)收集氢气与空气体积比为4:1的混合气体,其操作方法为________。
(3)用不同体积比的混合气体做氢气的燃烧实验,结果如表:
序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
氢气与空气体积比 | 9:1 | 8:2 | 7:3 | 5:5 | 3:7 | 1:9 | 0.5:9.5 |
点燃现象 | 安静 燃烧 | 安静 燃烧 | 弱的 爆鸣声 | 强的 爆鸣声 | 强的 爆鸣声 | 弱的 爆鸣声 | 不燃烧 不爆鸣 |
请分析上表信息,你对燃烧或燃烧条件的新认识是可燃物能否燃烧除具备燃烧条件,还要考虑到________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组为了测定贝壳中碳酸钙的质量分数,做如下实验:取贝壳样品12g装入烧杯中,向其中加入一定质量分数的稀盐酸(杂质不溶于水也不参加反应),所加盐酸的质量与烧杯中剩余固体质量关系如下图。试计算:
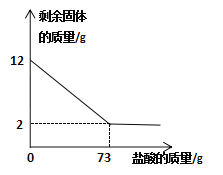
(1)贝壳中碳酸钙的质量为________g
(2)稀盐酸中溶质的质量分数______。(写出计算过程)
(3)恰好完全反应时,所得溶液中溶质的质量分数______。(计算精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钠是日常生活的必需品,也是重要的化工原料。
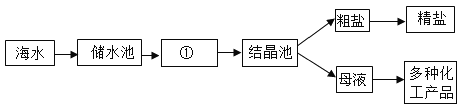
(1)下图是利用海水提取粗盐的过程:上图中①是_____池(填“蒸发”或“冷却”)。
(2)粗盐进行精制,流程如下图所示。粗盐除含 NaCl 外,还含有少量 MgCl2、CaCl2、Na2SO4 以及泥沙等杂质。某同学将该粗盐样品进行提纯。
提供的试剂:ABaCl2 溶液、BNa2CO3 溶液、CK2CO3 溶液、DNaOH 溶液。
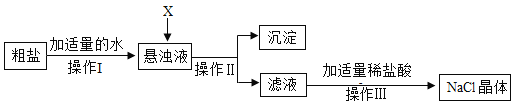
①欲除去悬浊液中的 MgCl2、CaCl2、Na2SO4,从提供的试剂中选出 X 所代表的试剂,按滴加顺序依次为:过量的_____(填序号)。
②操作Ⅱ的名称是_____,此操作使用玻璃棒的作用是_____,通过此操作得 到的滤液中除了有 NaCl 外,还含有的溶质有_____(填化学式)。
③加适量盐酸过程中,发生反应的化学方程式为_____(非中和反应)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2011年8月,云南曲靖市发生铬渣非法倾废致污事件,严重影响到珠江流域水质。铬元素是人体必需的微量元素,但铬过量会引起污染,危害人体健康。
(1)六价铬(Cr)对人体有毒,含铬废水要经化学处理后才能排放,具体的操作方法是:①加入一定量的绿矾(FeSO4·7H2O)把废水中的正六价铬转化成正三价铬离子;②加入过量的石灰水,使铬离子转变为氢氧化铬沉淀,则氢氧化铬的化学式为______;③再通过_____等基本操作除去沉淀物。
(2)不同价态的铬毒性不一样,其中六价铬的毒性最大,六价铬为吞入性和吸入性极毒物,若人体内六价铬超标,需要服用蔬菜和水果中富含的_____来缓解毒性。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属钛(Ti)抗腐蚀性能好,露置于空气中数年,仍光亮如初。以金红石(主要成分是TiO2)为原料生产金属钛的步骤主要有:①在高温下,向金红石与焦炭的混合物中通入氯气(Cl2),得到 TiCl4 和一种可燃性气体;②在稀有气体环境和加热条件下,用 Mg 和TiCl4 反应得到 Ti 和 MgCl2。下列说法不正确的是( )
A.①中的反应TiO2 +2C+2Cl2 TiCl4+2CO
TiCl4+2CO
B.②中的稀有气体的作用是隔绝空气,防止金属氧化
C.②中发生的反应为置换反应
D.金属钛在常温下极易与 O2 反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定石灰石中碳酸钙的质量分数,小明取石灰石样品,加到足量的稀盐酸中,进行实验(假定样品中其他成分不与稀盐酸反应)。
石灰石样品的质量 | 烧杯和稀盐酸的总质量 | 反应后烧杯及烧杯中各物质的总质量 |
12.5g | 87.5g | 95.6g |
请计算:
(1)生成二氧化碳的质量______________。
(2)求样品中碳酸钙的质量分数________________(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com