
【题目】某化学兴趣小组进行溶液的配制实验.
配制![]() 质量分数为
质量分数为![]() 的氢氧化钠溶液.
的氢氧化钠溶液.
(1)计算:需要氢氧化钠固体的质量为________![]() ;水的体积为________
;水的体积为________![]() (水的密度近似看作
(水的密度近似看作![]() ).
).
(2)称量:调节托盘天平平衡后,将________放在托盘天平的左盘,称量其质量.然后再在右盘添加________.最后添加氢氧化钠固体,直至天平平衡.
(3)溶解:用筒量取所需的水,倒入装有氢氧化钠固体的烧杯里,用玻璃棒________,使其溶解,并冷却至室温.
(4)存储:把配制好的溶液装入试剂瓶,塞好橡皮塞并________,放到指定的地方.
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:初中化学 来源: 题型:
【题目】如图为晶体M(不含结晶水)的溶解度曲线,a、b两点分别表示M物质的溶液。下列有关说法或a、b间的转化方法错误的是( )
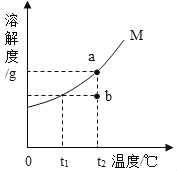
A. t2℃时,a点表示饱和溶液,b点表示不饱和溶液
B. 将a、b两份溶液温度降到t1℃时,仅a中有晶体析出
C. 从a→b:先将a降温到t1℃,然后再将溶液升温到t2℃
D. 从b→a:在b中加入过量M
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某溶液中可能含有Na2CO3、Na2SO4、NaHCO3三种物质中的一种或两种.为探究其组成,小明取出两份相同的样品溶液于试管中,向一份中加入过量的盐酸,产生无色气泡;向另一份中滴加过量的氯化钡溶液,产生白色沉淀.
![]() 、[发现问题]
、[发现问题]
Na2CO3、NaHCO3与过量的盐酸,均能产生无色气泡,Na2CO3、Na2SO4与过量的氯化钡溶液,均能产生白色沉淀.无法确定溶液的成份.
![]() 、[提出猜想]
、[提出猜想]
猜想1:溶液中只存在Na2CO3猜想2:________
猜想3:________猜想4:溶液中存在Na2SO4、NaHCO3
![]() 、[查阅资料]
、[查阅资料]
BaCO3溶于盐酸或硝酸,而BaSO4不溶于盐酸或硝酸,Ba(HCO3)2易溶于水,但在其溶液加入碱可生成BaCO3沉淀,加酸产生无色气泡.
![]() 、[设计实验]
、[设计实验]
用胶头滴管取少量溶液加入试管中,再用滴管取过量的氯化钡溶液并滴加到试管![]() 中,充分反应后,静置,然后过滤,将沉淀和滤液分别装入另外的两个试管中;往装有沉淀的试管中加入过量的稀盐酸;往装有滤液的试管中加入稀盐酸.
中,充分反应后,静置,然后过滤,将沉淀和滤液分别装入另外的两个试管中;往装有沉淀的试管中加入过量的稀盐酸;往装有滤液的试管中加入稀盐酸.
![]() 、[实验现象]
、[实验现象]
沉淀不溶解,出现无色气泡.
![]() 、[结论]________.
、[结论]________.
![]() 、[反思与评价]
、[反思与评价]
![]() 除去溶液中少量杂质时,往溶液中加入适量________(填化学式)溶液.
除去溶液中少量杂质时,往溶液中加入适量________(填化学式)溶液.
![]() 检验时加入氯化钡溶液,同时加入稀硝酸的原因是________.
检验时加入氯化钡溶液,同时加入稀硝酸的原因是________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】室温下,将甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如图1所示,甲、丙固体有剩余,乙固体全部溶解.升温到80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化.
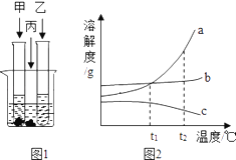
(1)室温时,________(填“甲”、“乙”或“丙”)溶液可能是不饱和溶液.
(2)若甲中含有少量丙,应用________法提纯.
(3)图2中能表示乙物质的溶解度曲线的是________(填“a”、“b”或“c”).
(4)t2℃时,甲、乙、丙三种物质等质量的饱和溶液中水的质量由大到小的顺序是________.
(5)t2℃时,甲、乙、丙三种物质等质量的饱和溶液降温至t1℃时,所得甲、乙、丙三种溶液的溶质质量分数大小关系________(用甲、乙、丙表示).
(6)若用质量分数为6%的甲溶液配制150g质量分数为2%的甲溶液,需加水________g;主要实验步骤为计算、________、混匀.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在农业生产中,常常要用质量分数为![]() 的食盐溶液来选种.
的食盐溶液来选种.
![]() 为什么用
为什么用![]() 的食盐溶液而不用水________.
的食盐溶液而不用水________.
![]() 实验室要配制
实验室要配制![]() 这种食盐溶液,需要食盐________
这种食盐溶液,需要食盐________![]() ,水________
,水________![]() .
.
![]() 实验室有以下仪器:①药匙②集气瓶③烧杯④试管⑤玻璃棒⑥量筒⑦胶头滴管⑧铁架台⑨酒精灯⑩托盘天平,配制此溶液所需的仪器有(填编号)________.
实验室有以下仪器:①药匙②集气瓶③烧杯④试管⑤玻璃棒⑥量筒⑦胶头滴管⑧铁架台⑨酒精灯⑩托盘天平,配制此溶液所需的仪器有(填编号)________.
![]() 在配制溶液的过程中,有以下操作:①加水溶解食盐固体②称量食盐固体③搅拌加速溶解④计算⑤用量筒量取水,其中正确的操作顺序(填编号)是________.
在配制溶液的过程中,有以下操作:①加水溶解食盐固体②称量食盐固体③搅拌加速溶解④计算⑤用量筒量取水,其中正确的操作顺序(填编号)是________.
![]() 若配制的食盐溶液的质量分数经检验小于
若配制的食盐溶液的质量分数经检验小于![]() ,试分析造成误差的可能原因.(至少写三条)________、________、________.
,试分析造成误差的可能原因.(至少写三条)________、________、________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】规范操作和认真细致的实验习惯是有效开展化学实验的关键。
(1)试管是实验室最常见的仪器,如图所示,在不同的化学实验中试管口的朝向不同.下列说法中正确的是____________(填序号)。
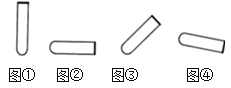
a.给试管中的液体加热时,试管口朝向如图①
b.向试管中加入块状固体时,试管口朝的向先如图②后如图①
c.给试管中的固体加热时,试管口朝向如图④
d.用胶头滴管向试管中滴加液体时,试管口朝向如图③
(2)根据下图,读出液体的体积为________m L;精盐质量是_______g。
![]()

![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明暑假期间到农田施肥时,发现撒落在地上的碳铵(碳酸氢铵的简称)在阳光的照射下很快消失了,同时有浓烈的刺激性气味.他很好奇,返校后和同学们进行探究,请你一同参与:
(提出问题)碳酸氢铵很快消失,这一过程是物理变化还是化学变化?
(查阅资料)

![]() 纯净的碳铵是一种无味、易溶于水的白色固体.其特点是在低温、干燥的条件下,能稳定存在.但是,当温度稍高(10℃以上)或湿度稍大,碳铵就易消失;碳铵不能使湿润的酚酞试纸变红色.
纯净的碳铵是一种无味、易溶于水的白色固体.其特点是在低温、干燥的条件下,能稳定存在.但是,当温度稍高(10℃以上)或湿度稍大,碳铵就易消失;碳铵不能使湿润的酚酞试纸变红色.
(2)二氧化碳气体能使澄清的石灰水变浑浊,常用于检验二氧化碳气体.碳酸氢铵也能使澄清石灰水变浑浊.
(3)氨气能使湿润的酚酞试纸变红色,常用于检验氨气(NH3).
(收集证据)(1)按如图所示安装好实验装置,安装仪器的顺序是________
![]() 检查装置的气密性,检查方法是________
检查装置的气密性,检查方法是________
![]() 进行实验:
进行实验:
实验步骤 | 实验现象 | 实验结论 |
①在试管中加入少量碳铵粉末,加热.将一白瓷板放在导管口的下方 | ||
②将湿润的酚酞试纸与碳铵接触 | 酚酞试纸没有颜色变化 | 碳铵不能使酚酞试纸变红 |
③将湿润的酚酞试纸放于试管口处 |
(获得结论)碳铵受热消失了,生成了新物质,发生了化学变化.
(反思与交流)![]() 实验时小王同学的试管内壁附有碳铵粉末,你的建议是________;小刘同学的试管破裂了,你认为原因可能是(写一条)________.
实验时小王同学的试管内壁附有碳铵粉末,你的建议是________;小刘同学的试管破裂了,你认为原因可能是(写一条)________.
![]() 有的同学认为上述实验不需要做碳铵能否与湿润的酚酞试纸作用的实验,你同意吗?为什么?________.
有的同学认为上述实验不需要做碳铵能否与湿润的酚酞试纸作用的实验,你同意吗?为什么?________.
![]() 闻生成物的气味时有的同学直接把鼻子凑到试管口处,结果受到了比较强烈的刺激,你认为正确的做法是________.对于如何减少实验过程中生成气体的强烈刺激,你的建议是________
闻生成物的气味时有的同学直接把鼻子凑到试管口处,结果受到了比较强烈的刺激,你认为正确的做法是________.对于如何减少实验过程中生成气体的强烈刺激,你的建议是________
![]() 有的同学把导气管通入到澄清的石灰水,石灰水变浑浊,他认为由此也可说明生成了二氧化碳,发生了化学变化,你认为理由充分吗?为什么? ________
有的同学把导气管通入到澄清的石灰水,石灰水变浑浊,他认为由此也可说明生成了二氧化碳,发生了化学变化,你认为理由充分吗?为什么? ________
![]() 根据以上实验,你认为碳酸氢铵化肥在存放时应注意的问题是________.
根据以上实验,你认为碳酸氢铵化肥在存放时应注意的问题是________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示实验填空。

(1)如图A所示,在盛有水的小烧杯中滴入几滴红墨水,一段时间后,小烧杯中的现象是____________________,说明________________________。
(2)用两个相同体积的注射器分别吸取5 mL空气和5 mL红墨水,如图B所示。用手指顶住末端注射孔,然后向内推活塞,比较推动活塞的难易程度。该实验验证了:
①分子之间有____________。
②________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
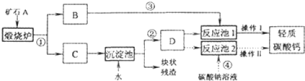
【题目】用作牙膏摩擦剂的轻质碳酸钙可以用矿石![]() 来制备,某化学兴趣小组设计了
来制备,某化学兴趣小组设计了![]() 种转化流程,如图所示.
种转化流程,如图所示.
(生产流程)
(相关资料)
![]() .二氧化碳持续通入氢氧化钙溶液发生如下反应:
.二氧化碳持续通入氢氧化钙溶液发生如下反应:
![]() ,
,![]() ;
;
![]() .碳酸氢钙微溶于水,微热易分解:
.碳酸氢钙微溶于水,微热易分解:![]() ;
;
![]() .生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆.
.生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆.
(问题讨论)
![]() 小王主张用流程①、②、④和操作
小王主张用流程①、②、④和操作![]() 的设计.请写出反应①和④的化学方程式:
的设计.请写出反应①和④的化学方程式:
①________;④________;
操作![]() 包括搅拌和________、洗涤、烘干等工序;该流程中,通过反应④可回收副产品_____.
包括搅拌和________、洗涤、烘干等工序;该流程中,通过反应④可回收副产品_____.
![]() 小李认为流程①、②、③和操作
小李认为流程①、②、③和操作![]() 比小王的主张更好,理由是:________;
比小王的主张更好,理由是:________;
![]() 制轻质碳酸钙时,
制轻质碳酸钙时,![]() 为________(选填“悬浊液”或“溶液”),理由是:________.
为________(选填“悬浊液”或“溶液”),理由是:________.
![]() 小李认为得到的产品中可能含有杂质
小李认为得到的产品中可能含有杂质![]() ,所以操作
,所以操作![]() 包括搅拌、________和过滤、烘干等工序,以提高产率.
包括搅拌、________和过滤、烘干等工序,以提高产率.
(产品含量测定)![]() 含量的测定:取
含量的测定:取![]() 产品,研成粉状后,按图进行实验.
产品,研成粉状后,按图进行实验.
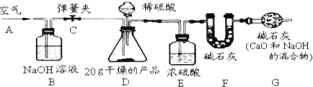
![]() 实验步骤:
实验步骤:
①连接好装置,检查气密性;②打开弹簧夹![]() ,在
,在![]() 处缓缓通入一段时间空气;
处缓缓通入一段时间空气;
③称量![]() 的质量;④关闭弹簧夹
的质量;④关闭弹簧夹![]() ,慢慢滴加稀硫酸至过量,直至
,慢慢滴加稀硫酸至过量,直至![]() 中无气泡冒出;
中无气泡冒出;
⑤打开弹簧夹![]() ,再次缓缓通一段时间空气;⑥称量
,再次缓缓通一段时间空气;⑥称量![]() 的质量,得前后两次质量差为
的质量,得前后两次质量差为![]() .
.
![]() 问题探究
问题探究
①产品研成粉的目的________;
②![]() 装置的作用是________;
装置的作用是________;![]() 装置的作用是________,
装置的作用是________,
③若没有![]() 装置,则测定的
装置,则测定的![]() 的质量分数会________(填“偏大”、“偏小”、“不变”).
的质量分数会________(填“偏大”、“偏小”、“不变”).
称量![]() 的质量,得前后两次质量差为
的质量,得前后两次质量差为![]() ,可求得产品中
,可求得产品中![]() 的质量分数为________
的质量分数为________![]() .
.
(总结反思)
某同学设计上述实验方案测定牙膏中钙元素的质量分数:向一定量牙膏中加入过量稀盐酸,测定生成![]() 的质量,据此计算牙膏中钙元素的质量分数.小李同学认为即使排除实验仪器和操作的影响,上述测定的结果仍不一定准确,理由是________.
的质量,据此计算牙膏中钙元素的质量分数.小李同学认为即使排除实验仪器和操作的影响,上述测定的结果仍不一定准确,理由是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com