
 孔雀石[碱式碳酸铜,主要成分是Cu2(OH)2CO3]具有色彩浓淡的条状花纹(如图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.
孔雀石[碱式碳酸铜,主要成分是Cu2(OH)2CO3]具有色彩浓淡的条状花纹(如图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.
| ||
| ||
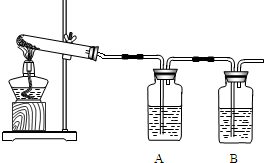
| 操作和药品 | 现象 | 分析和结论 | |
| 方案Ⅰ | 取少量剩余黑色粉末,充分灼烧 | ①______________ ________________ |
原剩余黑色粉末是 氧化铜 |
| 方案Ⅱ | ②_______________ __________________ |
③_____________ _________________ |
原剩余黑色粉末是 氧化铜 |
| 配方1 | 配方2 | 配方3 | 配方4 | |
| 木炭质量(g) | 0.4 | 0.5 | 0.6 | 0.7 |
| 氧化铜质量(g) | 8 | 8 | 8 | 8 |


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2012-2013学年辽宁省鞍山市中考一模化学试卷(解析版) 题型:计算题
某科研小组预测定孔雀石中碱式碳酸铜[Cu2(OH)2CO3]的质量分数.现称取30g该孔雀石样品放入烧杯中,再逐滴加入稀盐酸至恰好完全反应,反应的化学方程式为:铜Cu2(OH)2CO3+4HCl=2CuCl2+CO2↑+3H2O.共消耗该稀盐酸146g(假设杂质不与稀盐酸反应,也不溶于水),最终称得烧杯中剩余物质的质量为171.6g.试求:
(1)孔雀石中碱式碳酸铜的质量分数;
(2)所得溶液中溶质的质量分数.(结果保留至0.1%)
查看答案和解析>>
科目:初中化学 来源:2011-2012学年北京市顺义区九年级(上)期末化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com