
某化学兴趣实验小组得到一个失去标签的药品.它是一包白色粉末,据分析可能是碳酸钠,也可能是氧化钙或氢氧化钙.为确定其组成,他们设计了以下实验方案进行探究,请你按要求帮助完成探究活动.
(1)提出假设:
假设①:白色粉末是碳酸钠;
假设②:白色粉末是氧化钙;
假设③:白色粉末是氢氧化钙.
(2)设计实验,通过实验分析进行判断并填空:

(3)实验后思考:假定这包白色粉末是混有少量氧化钙的碳酸钠粉末,将混合物溶于水可观察到的现象是________.
发生的两个反应为:
①________.
②________.
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
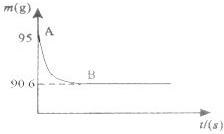 化学陈老师指导某化学兴趣学习小组进行了一个有趣的实验探究:测定鸡蛋壳的主要成分碳酸钙的质量分数.现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g稀盐酸,使之恰好完全反应(鸡蛋壳中杂质不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),试计算:
化学陈老师指导某化学兴趣学习小组进行了一个有趣的实验探究:测定鸡蛋壳的主要成分碳酸钙的质量分数.现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g稀盐酸,使之恰好完全反应(鸡蛋壳中杂质不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),试计算:查看答案和解析>>
科目:初中化学 来源: 题型:
化学老师张××指导某化学兴趣学习小组进行了一个有趣的实验探究:测定鸡
蛋壳的主要成分碳酸钙的质量分数。实验如下:将鸡蛋壳洗净、干燥并捣碎后,称取8.0g放在烧杯里,然后往烧杯中加入足量的稀盐酸50mL(密度1.1g/ml),充分反应后,称得反应剩余物为59.92g(假设其他物质不与盐酸反应)。请回答:
(1)上述稀盐酸的质量为 g,产生二氧气体的质量为 g。
(2)计算该鸡蛋壳中碳酸钙的质量分数。 (要求写出计算过程)
(3)该稀盐酸中HCI的质量分数应不小于多少?(要求写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com