
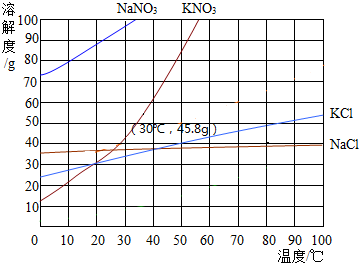
 如图为几种固体的溶解度曲线,回答下列问题:
如图为几种固体的溶解度曲线,回答下列问题:分析 根据题目信息和溶解度曲线可知:硝酸钾的溶解度随温度的升高而增大,在10℃时,NaNO3的溶解度为80g;某温度下,100g质量分数为30%的硝酸钠溶液中溶质质量=30g,稀释成质量分数为12%需要甲水的质量为x,(100g+x)×12%=30g,x=150g;30℃时,硝酸钾的溶解度是45.8g,向100g水中加入30g硝酸钾,所得溶液为不饱和溶液,将上述溶液蒸发掉50g水后恢复到30℃,析出的固体质量是15g;向A、B两个烧杯中各加入100g水,分别配成60℃的氯化钠和硝酸钾饱和溶液,再冷却到10℃,B烧杯中析出固体较多,因为硝酸钾比氯化钠受温度的影响变化大.
解答 解:(1)KNO3的溶解度随温度变化的规律是:硝酸钾的溶解度随温度的升高而增大;故答案为:硝酸钾的溶解度随温度的升高而增大;
(2)某温度下,100g质量分数为30%的硝酸钠溶液中溶质质量=30g,稀释成质量分数为12%需要甲水的质量为x,(100g+x)×12%=30g,x=150g;故答案为:10;150;
(3)30℃时,硝酸钾的溶解度是45.8g,向100g水中加入30g硝酸钾,所得溶液为不饱和溶液,将上述溶液蒸发掉50g水后恢复到30℃,析出的固体质量是15g;故答案为:不饱和;15;
(4)向A、B两个烧杯中各加入100g水,分别配成60℃的氯化钠和硝酸钾饱和溶液,再冷却到10℃,B烧杯中析出固体较多,因为硝酸钾比氯化钠受温度的影响变化大;故答案为:B;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的计算等,有关的计算要准确,本考点主要出现在选择题和填空题中.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 盐水是纯净物 | B. | 硬水通过蒸馏可以转化为软水 | ||
| C. | 水电解属于物理变化 | D. | 水污染与人类活动无关 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
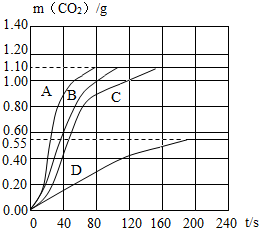
| 实验 编号 | 温度(℃) | 大理石 规格 | 盐酸浓度(均取100mL) | 实验目的 |
| ① | 20 | 粗颗粒 | 20% | (Ⅰ)实验①和②探究盐酸浓度对该反应速率的影响; (Ⅱ)实验①和④探究温度对该反应速率的影响; (Ⅲ)实验①和③探究大理石规格(粗、细)对该反应速率的影响; |
| ② | 20 | 粗颗粒 | 10% | |
| ③ | 细颗粒 | 20% | ||
| ④ | 粗颗粒 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
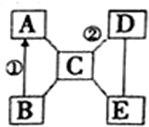 A、B、C、D、E是初中化学常见的五种不同类别的物质,其中B为红色固体,C是胃液的主要成分,E俗称苏打.图中“-”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去.
A、B、C、D、E是初中化学常见的五种不同类别的物质,其中B为红色固体,C是胃液的主要成分,E俗称苏打.图中“-”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 维生素和蛋白质 | B. | 无机盐和油脂 | C. | 蛋白质和糖类 | D. | 维生素和糖类 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
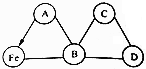 已知A、B、C、D为初中化学中常见的四种不同类别的化合物,且C和D的水溶液均显碱性.它们与铁存在如图所示反应和转化关系(“-”表示相连两种物质之间可发生反应,箭头表示转化关系,反应条件、部分反应物和生成物已略去).
已知A、B、C、D为初中化学中常见的四种不同类别的化合物,且C和D的水溶液均显碱性.它们与铁存在如图所示反应和转化关系(“-”表示相连两种物质之间可发生反应,箭头表示转化关系,反应条件、部分反应物和生成物已略去).查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 玉堂陈醋是混合物,它的有效成分是醋酸 | |
| B. | 醋酸有2个碳原子、4个氢原子和2个氧原子构成 | |
| C. | 醋酸是由碳、氢、氧三种元素组成的化合物,其元素个数比为1:2:1 | |
| D. | 醋酸是一种有机物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氮气的化学性质稳定可作保护气 | B. | 氧气有助燃性可作燃料 | ||
| C. | 室内燃气泄漏应立即打开排风扇 | D. | 用过滤的方法将硬水转化成软水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com