
 水-生命之源
水-生命之源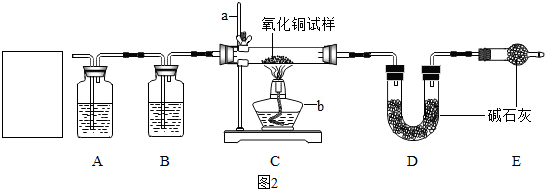
分析 (1)利用肥皂水可以区分硬水和软水,加热煮沸可以降低水的硬度;
(2)化合物中元素化合价代数和为零;
(3)利用pH试纸可以测定溶液的酸碱度;
(4)电解水时,正极产生的是氧气,负极产生的是氢气,氧气和氢气的体积比约为1:2;
(5)锌和稀盐酸反应生成氯化锌和氢气;
氢氧化钠溶液能够吸收氯化氢气体,浓硫酸可以用来干燥氢气;
加热条件下,氧化铜和氢气反应生成铜和水;
根据提供的数据可以计算水中氢氧原子个数比;
根据提供的数据和反应的化学方程式可以计算完成此实验至少需要纯度为80%的粗锌的质量.
解答 解:(1)向水中加入肥皂水时,如果产生的泡沫较多,是软水,如果产生大量浮渣,是硬水;
加热煮沸时,水中的钙离子、镁离子能够以碳酸钙沉淀、氢氧化镁沉淀的形式从水中析出,从而降低水的硬度.
故填:肥皂水;加热煮沸.
(2)二氧化氯中,氧元素的化合价是-2,根据化合物中元素化合价代数和为零可知,氯元素的化合价是+4,可以表示为$\stackrel{+4}{Cl}$O2.
故填:$\stackrel{+4}{Cl}$O2.
(3)某养殖场欲测定水池中水的酸碱性强弱,可选用pH试纸.
故填:C.
(4)化学上用如图1装置来测定水的组成,其中a为电源的负极;
设电解水的水的质量为x,
根据题意有:$\frac{0.3g}{0.3g+49.7g-x}$×100%=0.625%,
x=2g,
乙试管中收集的气体是氧气,设生成氧气的质量为y,
2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,
36 32
2g y
$\frac{36}{2g}$=$\frac{32}{y}$,
y=1.8g,
该实验得到关于水的组成的结论是水由氢元素和氧元素组成.
故填:负;1.8;水由氢元素和氧元素组成.
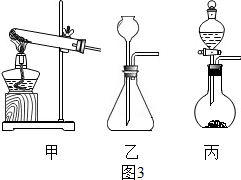
(5)①a是铁架台,b是酒精灯.
故填:铁架台;酒精灯.
②本次实验中用锌和较浓的盐酸反应并得到持续稳定的气流,方框中应当选用的发生装置为丙,其中生成氢气的化学方程式为:Zn+2HCl═ZnCl2+H2↑.
故填:丙;Zn+2HCl═ZnCl2+H2↑.
③图中A、B装置中放的药品分别是氢氧化钠溶液和浓硫酸,用来吸收氯化氢气体和干燥氢气.
故填:c.
④实验开始通一段时间的氢气,目的是除尽装置中的空气,确认此目的已经达到的实验操作方法为在E装置尾部收集气体验纯,如果氢气已经纯净,则空气被排尽.
故填:在E装置尾部收集气体验纯.
⑤加热一段时间后,C中发生反应的方程式为:CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
实验结束后,停止加热,继续通氢气的目的之一是让生成的铜充分冷却,另一目的为使反应生成的水被完全吸收.
故填:CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;使反应生成的水被完全吸收.
⑥E装置的作用为防止空气中的水蒸气和二氧化碳被D装置吸收;
若无此装置,会导致水的质量偏大,从而导致氢元素质量偏大,进一步导致实验测得的氢氧个数比偏大.
故填:防止空气中的水蒸气和二氧化碳被D装置吸收;偏大.
⑦反应生成水的质量为:121.8g-120.0g=1.8g,
水中氢元素质量为:1.8g×$\frac{2}{18}$×100%=0.2g,
水中氧元素质量为:101.6g-100.0g=1.6g,
计算该实验方法测得的氢氧个数比为:$\frac{0.2g}{1}$:$\frac{1.6g}{16}$=2:1.
故填:2:1.
⑧A.氧化铜没有全部被还原,不会影响实验过程中氢氧原子个数比测定;
B.氧化铜中混有杂质氧化铁,不会影响实验过程中氢氧原子个数比测定;
C.氧化铜未完全干燥,会导致实验过程中氢氧原子个数比偏大;
D.氧化铜中混有少量氢氧化铜时,氢氧化铜受热分解生成氧化铜和水,会导致实验过程中氢氧原子个数比偏大.
故填:AB.
⑨设参加反应的锌质量为m,
由Zn+2HCl═ZnCl2+H2↑,CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O可知,Zn~H2O,
Zn~H2O,
65 18
m 1.8g
$\frac{65}{m}$=$\frac{18}{1.8g}$,
m=6.5g,
若本次实验中需要的锌的质量为:6.5g÷$\frac{1}{5}$=32.5g,
则完成此实验至少需要纯度为80%的粗锌质量为:32.5g÷80%=40.625g,
答:完成此实验至少需要纯度为80%的粗锌质量为40.625g.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:选择题
| A. | 生产生活中,可用加热高锰酸钾的方法制得大量的氧气 | |
| B. | 鱼类能在水中生存,证明氧气极易溶于水 | |
| C. | 木炭在空气中灼烧红热,在氧气中燃烧并发出白光,现象不同与氧气的浓度有关 | |
| D. | 空气中氧气的质量分数约为21% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 橡胶鞋底 | B. | 尼龙背包 | C. | 塑料水瓶 | D. | 纯棉毛巾 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②⑤⑥ | C. | ①③⑤ | D. | ②④⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 解释 |
| A | 洗涤剂能去除衣服上的油污 | 洗涤剂具有乳化作用 |
| B | 二氧化碳能使紫色石蕊试液变红 | 二氧化碳具有酸性 |
| C | 温度计中的水银能指示温度 | 汞原子间距离随温度升高而增大 |
| D | 打开汽水瓶盖时,汽水会自动喷出 | 气体的溶解度随压强减小而减小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com