
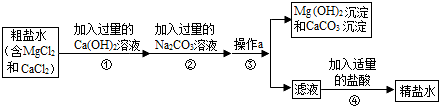
���� ��1������������Һ���Ȼ�þ��Ӧ����������þ�������Ȼ��ƣ�
��2��̼�������Ȼ��Ʒ�Ӧ����̼��Ƴ������Ȼ��ƣ�̼������������������Ʒ�Ӧ����̼��Ƴ������������ƣ�
��3�����ݹ����Ƿ����Һ�����IJ����������ڷ�Ӧ�е����������
��4������ʳ��ˮʱ��Ҫ������������̨���ƾ��ơ���������������ȣ��������������е�ע�����������
��� �⣺��1������������Һ���Ȼ�þ��Ӧ����������þ�������Ȼ��ƣ�����ʽΪ��MgCl2+Ca��OH��2=Mg��OH��2��+CaCl2��
��2��̼�������Ȼ��Ʒ�Ӧ����̼��Ƴ������Ȼ��ƣ�̼������������������Ʒ�Ӧ����̼��Ƴ������������ƣ�����ʽΪ��Na2CO3+CaCl2=CaCO3��+2NaCl��Ca��OH��2+Na2CO3�TCaCO3��+2NaOH��
��3��������ǹ��˰ѳ���������þ��̼��Ƴ������˷��룬�䲣����������������������ܼ������������Ŀ���dz�ȥ��Һ�е�Na2CO3���������ƣ�
��������ˮʱ�����ֽ϶����ʱ��ֹͣ���ȣ�
��4������ʳ��ˮʱ��Ҫ������������̨���ƾ��ơ������������������������������ˮʱ�����ֽ϶����ʱ��ֹͣ���ȣ�
�𰸣���1��MgCl2+Ca��OH��2=Mg��OH��2��+CaCl2��
��2��Na2CO3+CaCl2=CaCO3��+2NaCl��Ca��OH��2+Na2CO3�TCaCO3��+2NaOH��
��3�����ˣ��������������ƣ�
��4����������������Һ���У�
���� ���ᴿ�Ǿ�����������ݣ�����Ҫ�漰����ѧ����ʽ����д�����˲��������ʵij�ȥ�����ݣ���Ҫͬѧ�ǶԴ�������Ȼ���ģ�


 �����߿����ϵ�д�
�����߿����ϵ�д� �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д� Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ȼ�� | B�� | ʯ��ȼ�� | C�� | ���������� | D�� | ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ����Һ | NaCl | Na2C03 | BaCl |
| pH | ����7 | ����7 | ����7 |
| ʵ�鲽�� | ʵ������ | ʵ����� |
| ��1��ȡ��������Һ���Թ��У�����Һ�еμ��������Ȼ�����Һ���������� | �а�ɫ�������� | ˵��ԭ����Һ��һ�����е�������̼���ƣ� |
| ��2�����裨1����ַ�Ӧ�����Һ�еμӷ�̪��Һ�� | ��Һ��ɺ�ɫ | ˵��ԭ����Һ�л�һ�������������ƣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
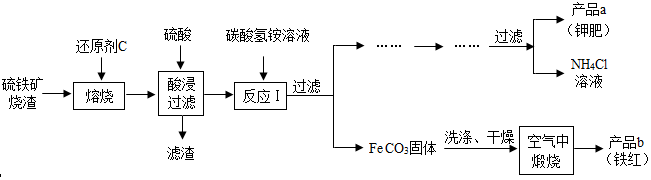
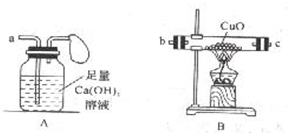
 ̼�����׳ƴ����¶�ڿ����п�������еĶ�����̼��ˮ������Ӧ��Na2CO3+CO2+H2O�T2NaHCO3����һƿ���õ�̼���ƣ����к���̼�����ƣ���Ϊ�˲ⶨ����̼���Ƶ��������������������ʵ�鷽����
̼�����׳ƴ����¶�ڿ����п�������еĶ�����̼��ˮ������Ӧ��Na2CO3+CO2+H2O�T2NaHCO3����һƿ���õ�̼���ƣ����к���̼�����ƣ���Ϊ�˲ⶨ����̼���Ƶ��������������������ʵ�鷽�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
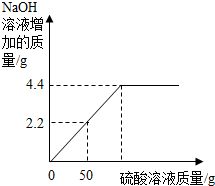 ��þ�����Ҫ�ɷ���MgCO3��Ϊ�˷���ij��þ����þԪ�صĺ�����ijѧϰС�������ʵ���о���ȡ10g��þ������δ֪Ũ�ȵ�H2SO4��Һ�����ɵ�����ȫ����NaOH��Һ���գ�����������Һ��������NaOH��Һ���ӵ������仯��ϵ��¼����ͼ����þ���е����ʲ�����ˮ�������ᷢ����Ӧ������
��þ�����Ҫ�ɷ���MgCO3��Ϊ�˷���ij��þ����þԪ�صĺ�����ijѧϰС�������ʵ���о���ȡ10g��þ������δ֪Ũ�ȵ�H2SO4��Һ�����ɵ�����ȫ����NaOH��Һ���գ�����������Һ��������NaOH��Һ���ӵ������仯��ϵ��¼����ͼ����þ���е����ʲ�����ˮ�������ᷢ����Ӧ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com