
| 选 项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | CO2(CO) | 通入足量的氧气,点燃 |
| B | CaO(CaCO3) | 加水溶解、过滤 |
| C | CO(CO2) | 循环通过灼热的炭粉 |
| D | KCl(MnO2) | 加足量水溶解后,过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、除去二氧化碳中的一氧化碳不能够通氧气点燃,这是因为除去气体中的气体杂质不能使用气体,否则会引入新的气体杂质,故选项所采取的方法错误.
B、CaO能与水反应生成氢氧化钙,碳酸钙难溶于水,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、CO2能与循环通过灼热的炭粉生成一氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、KCl易溶于水,MnO2难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故选项所采取的方法错误.
故选:C.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


 走进文言文系列答案
走进文言文系列答案科目:初中化学 来源: 题型:选择题
| A. | 用带火星的木条可以检验氧气 | |
| B. | 用加热高锰酸钾的方法可以制取氧气 | |
| C. | 鱼类能在水中生活,证明氧气易溶于水 | |
| D. | 红磷在氧气中燃烧,产生大量白烟 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 15g | B. | 18g | C. | 24g | D. | 36g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
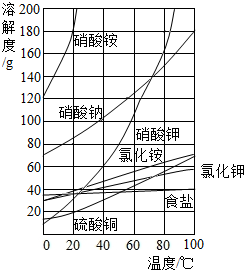 根据图中几种物质的溶解度曲线,回答下列问题:
根据图中几种物质的溶解度曲线,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
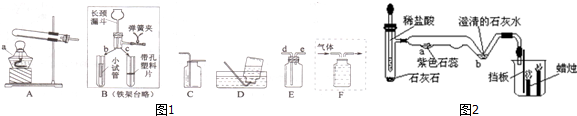
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
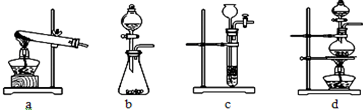
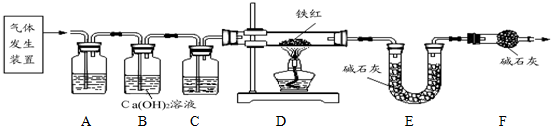
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 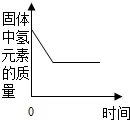 加热一定质量的高锰酸钾 加热一定质量的高锰酸钾 | |
| B. | 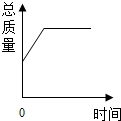 在密闭的容器中点燃一定质量的镁条 在密闭的容器中点燃一定质量的镁条 | |
| C. | 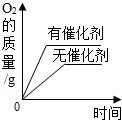 用等质量、等浓度的双氧水分别制取氧气 用等质量、等浓度的双氧水分别制取氧气 | |
| D. | 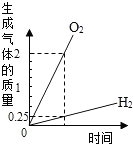 将水电解一段时间:无论任何时刻,氧气的质量:氢气的质量=8:1 将水电解一段时间:无论任何时刻,氧气的质量:氢气的质量=8:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子与原子的区别是分子可分而原子不可再分 | |
| B. | CO和CO2化学性质不同的原因是分子构成不同 | |
| C. | 合金的熔点肯定比其组成金属的熔点高 | |
| D. | 生铁和钢性能不同是因为含金属种类不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com