
将石灰石(CaCO3)在酒精喷灯火焰上高温煅烧.
(1)如何用实验事实证明石灰石已经开始分解?
(2)如何用实验事实证明石灰石没有完全分解?
|
答案:(1)将高温煅烧后的石灰石取少量投入试管中,加入水再滴入酚酞试液,若溶液变红,证明石灰石已经开始分解. (2)将高温煅烧后的石灰石取少量投入试管中,滴加少量稀盐酸,若有气体产生,说明石灰石没有完全分解;若没有气体产生,说明石灰石已完全分解. 分析:石灰石高温煅烧时发生分解反应,其化学方程式为:CaCO3 (1)要证明这个反应已经开始,只要证明生成物中有CaO或CO2存在即可.由于CO2不好收集,我们可以检验CaO的存在.CaCO3不溶于水,投入水中呈中性,CaO是碱性氧化物,投入水中可与水反应生成Ca(OH)2,溶液呈碱性. (2)要证明这个反应是否完全,只要证明反应物石灰石是否存在即可,如果石灰石完全分解了,石灰石就不应该存在了,可以用检验碳酸盐常用的方法来检验. |


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
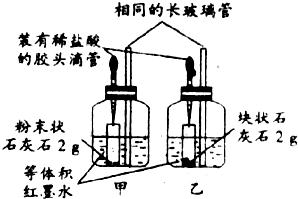 36、实验室一般用块状石灰石(大理石)和稀盐酸反应来制取二氧化碳,而不用粉末状石灰石(大理石)与稀盐酸反应制取二氧化碳、小杨、小柳、小梅三位同学对此进行探究.
36、实验室一般用块状石灰石(大理石)和稀盐酸反应来制取二氧化碳,而不用粉末状石灰石(大理石)与稀盐酸反应制取二氧化碳、小杨、小柳、小梅三位同学对此进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:
| 化学反应 | 化学方程式 | 简答 | ||||||||
| 电解水 | 2H2O
2H2O
|
与负极相连的玻璃管内产生的气体是 H2 H2 | ||||||||
| 高温煅烧石灰石 | CaCO3
CaCO3
|
将煅烧后的固体放入滴有酚酞的试液的水中,现象是 变红 变红 | ||||||||
| 无水硫酸铜与水反应 | CuSO4+5H2O=CuSO4?5H2O CuSO4+5H2O=CuSO4?5H2O |
现象是 水变蓝 水变蓝 | ||||||||
| 木炭和氧化铜反应 | C+2CuO
C+2CuO
|
该反应中的氧化剂是 CuO CuO | ||||||||
| 镁带在空气中燃烧 | 2Mg+O2
2Mg+O2
|
该反应中反应物的质量比 3:2 3:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com