
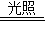 2H2O+4X↑+O2↑反应.
2H2O+4X↑+O2↑反应.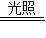 2H2O+4X↑+O2↑,推断硝酸见光会分解,得出硝酸保存在棕色瓶中的原因;
2H2O+4X↑+O2↑,推断硝酸见光会分解,得出硝酸保存在棕色瓶中的原因;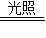 2H2O+4X↑+O2↑,利用反应前后原子种类、数目不变,推断生成物X的分子构成,写出物质X的化学式.
2H2O+4X↑+O2↑,利用反应前后原子种类、数目不变,推断生成物X的分子构成,写出物质X的化学式.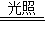 2H2O+4X↑+O2↑,硝酸在光照时会发生分解而变质;而棕色试剂瓶能避光而使瓶内硝酸避光保存;
2H2O+4X↑+O2↑,硝酸在光照时会发生分解而变质;而棕色试剂瓶能避光而使瓶内硝酸避光保存; 2H2O+4X↑+O2↑,反应前4HNO3中含有H、N、O原子个数分别为4、4、12,反应后2H2O、O2中含有H、N、O原子个数分别为4、0、4,根据反应前后原子种类、数目不变,则4X中含有4个N原子和8个O原子,每个X分子由1个N原子和2个O原子构成,其化学式为NO2;
2H2O+4X↑+O2↑,反应前4HNO3中含有H、N、O原子个数分别为4、4、12,反应后2H2O、O2中含有H、N、O原子个数分别为4、0、4,根据反应前后原子种类、数目不变,则4X中含有4个N原子和8个O原子,每个X分子由1个N原子和2个O原子构成,其化学式为NO2;

科目:初中化学 来源: 题型:
| ||
. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 2H2O+4X↑+O2↑反应.
2H2O+4X↑+O2↑反应.查看答案和解析>>
科目:初中化学 来源:江西 题型:填空题
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com