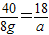(1)细铁丝在空气中不能燃烧,却能在氧气中燃烧,其燃烧现象是
很多物质在空气中的燃烧现象不如纯氧中剧烈,这说明了化学反应的剧烈程度与 有关.细铁丝燃烧后的生成物的质量比铁丝的质量 (填“增加”、“不变”“减少”)
(2)在2X+Y=Z+2R反应中,已知X、Y、Z的相对分子质量分别为20、49、71,若8gX恰好与Y完全反应,则生成R的质量是 克
(3)在4AB2+nC2═2A2C3+8BC2反应中,n的值是 .
【答案】
分析:根据已有的知识进行分析,铁丝能在氧气中燃烧,增大氧气的浓度能促进燃烧的进行;根据质量守恒定律即可进行有关的计算可判断,据此解答即可.
解答:解:(1)铁在氧气中能剧烈燃烧,火星四射,放出大量的热,生成黑色固体,增大反应物的浓度能促进反应的进行,铁燃烧后生成的是四氧化三铁,四氧化三铁的质量大于铁丝的质量,故填:剧烈燃烧,火星四射,生成黑色固体,放热,反应物浓度,增加;
(2)设R物质的相对分子质量为R
2X+Y=Z+2R
40 49 71
根据质量守恒定律则有:40+49=71+2R,解得R=9,
设生成R的质量为a
2X+Y=Z+2R
40 18
8g a
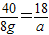
a=3.6g
故填:3.6
(3)4AB
2+nC
2═2A
2C
3+8BC
2反应中,反应前后各原子的个数不变,反应后C原子的个数是22,故反应前C原子的个数也是22,即n=11,故填:11.
点评:本题考查了氧气的有关化学性质以及化学用语的应用,完成此题,可以依据已有的知识进行.