
 ij���������ð�������Ĵ����Ʒ�к��������Ȼ������ʣ����Ʒ��װ����ע����̼���ơ�96%��Ϊ�ⶨ�ò�Ʒ�к�̼���Ƶ���������������������ʵ�飺ȡ11.00g������Ʒ�����ձ��У��Ƶ��ձ�����ʢ������Ʒ��������Ϊ158.00g���ٰ�100.00gϡ����ƽ���ֳ��ķ����μ�����Ʒ�У�ʵ�����ݼ�¼���£�
ij���������ð�������Ĵ����Ʒ�к��������Ȼ������ʣ����Ʒ��װ����ע����̼���ơ�96%��Ϊ�ⶨ�ò�Ʒ�к�̼���Ƶ���������������������ʵ�飺ȡ11.00g������Ʒ�����ձ��У��Ƶ��ձ�����ʢ������Ʒ��������Ϊ158.00g���ٰ�100.00gϡ����ƽ���ֳ��ķ����μ�����Ʒ�У�ʵ�����ݼ�¼���£�| ��������Ĵ��� | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
| ÿ�μ�����ǰ �ձ�����ʢ���ʵ�������/g | 158.00 | 181.24 | X | 228.60 |
| �����������Һ����/g | 25.00 | 25.00 | 25.00 | 25.00 |
| ��ַ�Ӧ���ձ�����ʢ����������/g | 181.24 | 204.48 | 228.60 | 253.60 |
| ÿ�����ɵĶ�����̼����/g | 1.76 | 1.76 | Y | 0 |
���� ǰһ��ʵ���г�ַ�Ӧ���ձ�����ʢ��������������һ�μ�������ǰ�ձ�����ʢ���ʵ�������������XΪ204.48g����y=204.48g+25.00g-228.60g=0.88g�����Կ�֪���ɵĶ�����̼��������Ϊ1.76g+1.76g+0.88g=4.40g�����ݻ�ѧ����ʽ����̼���Ƶ��������������������������������ݶ�����̼�������ƶϷ�Ӧ�������������
��� �⣺ǰһ��ʵ���г�ַ�Ӧ���ձ�����ʢ��������������һ�μ�������ǰ�ձ�����ʢ���ʵ�������������XΪ204.48g����y=204.48g+25.00g-228.60g=0.88g�����Կ�֪���ɵĶ�����̼��������Ϊ1.76g+1.76g+0.88g=4.40g��
��̼���Ƶ�����Ϊx
Na2CO3+2HCl�T2NaCl+H2O+CO2��
106 44
x 4.40g
$\frac{106}{44}$=$\frac{x}{4.40g}$
x=10.60g
�ò�Ʒ��̼���Ƶ���������Ϊ$\frac{10.60g}{11.00g}$��100%��96.4%��96%�ò�Ʒ�ϸ�
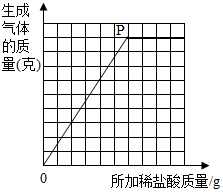
�������ݿ�֪��ÿ25g�����Ӧ�Ķ�����̼������Ϊ1.76g�������������0.88g������ֻ̼������12.5g��ϡ���ᣬ����ϡ���ᷴӦ������Ϊ25g+25g+12.5g=62.5g������P�������Ϊ��62.5��4.4��
�ʴ�Ϊ��
��1��204.48��
��2���ϸ�
��3����62.5��4.4����
���� ���ݻ�ѧ����ʽ����ʱ����һҪ��ȷ��д��ѧ����ʽ���ڶ�Ҫʹ����ȷ�����ݣ������������Ҫ������


 Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
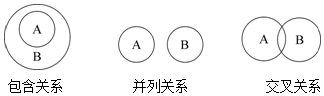
| A�� | ���������������ڰ�����ϵ | |
| B�� | �����������������ڲ��й�ϵ | |
| C�� | �����뻯�������ڽ����ϵ | |
| D�� | ����Ԫ����ǽ���Ԫ�����ڲ��й�ϵ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
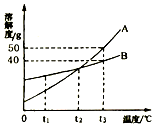 ��ͼ��A��B�������ʵ��ܽ�����ߣ���ش�
��ͼ��A��B�������ʵ��ܽ�����ߣ���ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
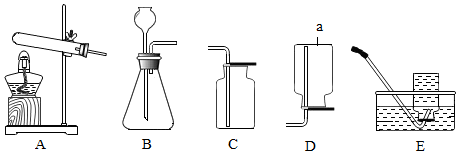
| A�� | �ڢ� | B�� | �ݢ� | C�� | �ڢۢ� | D�� | �ڢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
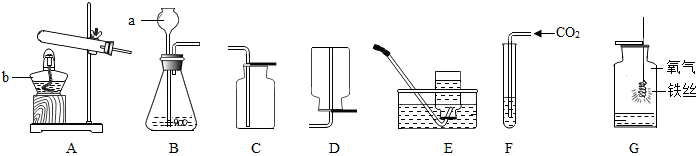
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com